| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《原电池原理》考点强化练习(2019年押题版)(十)
参考答案:B 本题解析:锌比铜活泼,所以锌是负极,失去电子,铜是正极,溶液中的氢离子得到电子,所以选项B不正确,溶液中不可能传递电子,电子是通过导线传递的,其余选项都是正确的,答案选B。 本题难度:一般 2、选择题 下列有关电池的说法错误的是 |
参考答案:C
本题解析:锂离子电池可以反复充放电,属于二次电池,A正确;铅蓄电池中负极为铅,正极是二氧化铅,电解质是硫酸,B正确;原电池中负极失去电子,正极得到电子。则氢氧燃料电池正极输入空气,负极输入氢气,C不正确。干电池中的电解质溶液易与锌反应减小电解质的量和电极材料的量,所以锌锰干电池即使不用,长久放置也会失效,D正确,答案选C。
考点:考查常见电池的判断
点评:该题紧密联系生活实际,基础性强,难度不大,有利于调动学生的学习兴趣,激发学生的学习积极性。
本题难度:一般
3、选择题 肼(N2H4)―空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。下列说法中,不正确的是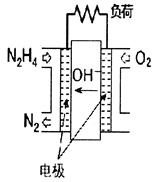
A.该电池放电时,通入肼的一极为负极
B.电池每释放1mol N2转移的电子数为4NA
C.通入空气的一极的电极反应式是:O2+2H2O+4e-=4OH-
D.电池工作一段时间后,电解质溶液的pH将不变
参考答案:D
本题解析:原电池中负极失去电子,所以肼在负极通入,A正确。肼中氮元素的化合价是-2价,氧化产物是氮气,所以每释放1mol N2转移的电子数为4NA,B正确。氧气在正极通入,C正确。由于总反应式为N2H4+O2=N2+2H2O,所以氢氧化钾的浓度会降低,pH减小,D不正确。答案选D。
本题难度:一般
4、填空题 (6分)从铜、铁及碳棒中选取合适的电极材料设计一个原电池,实现反应:
2FeCl3+Cu=2FeCl2+CuCl2
负极为?,电极反应方程式为?,
正极应选?,电极反应方程式为?。
参考答案:Cu(1分)? Cu-2e-=Cu2+?(2分)
C?(1分)? 2Fe3++2e-=2Fe2+(2分)
本题解析:略
本题难度:一般
5、选择题 在下图所示的原电池中,正极发生的反应是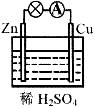
A.2H++2e
参考答案:
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《微量元素》.. | |