1������� (12��)��1�����ʵ���Ũ����ͬ��������NX��NaY��NaZ����Һ����pH����Ϊ8��9��10����HX��HY��HZ��������ǿ������˳���� ��
��2���Ƚ�������Һ��pH(�>����<����=��)��
��0��1 mol��L-1Na2CO3��Һ 0��1 mol��L-1NaHCO3��Һ
��0��1 mol��L-1NH4Cl��Һ 0��01 mol��L-1NH4C1��Һ
��3����a��b��c��d�Ŀ����Ƭ������ϡH2SO4�У��õ�������������������ɸ���ԭ��ء���a��b������aΪ������c��d������c������������Ӧ��a��c������cΪ������b��c������������c������b�����������ֽ����Ļ����ǿ������˳��Ϊ ��
��4����AlCl3��Һ���ɡ����գ�������õĹ������Ҫ�ɷ��� ��
��5���Ȼ�����Һ�� ��(��ᡱ��������С�)��ԭ����(�����ӷ���ʽ��ʾ)��
��6����������Һ����μ���Ba(OH)2��Һ��SO42-�պó�����ȫʱ����Һ��pH 7(�>����<����=��)�����ӷ�Ӧ�ܷ���ʽΪ�� ��
�ο��𰸣���1��HX>HY>ZH����2���� > ��> ����3��a >b>c>d ����4�� Al2O3����5�����ԣ�Fe3++3H2O Fe(OH)3+3H+����6�� < ��Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4��+2H2O��
Fe(OH)3+3H+����6�� < ��Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4��+2H2O��
�����������1�����ʵ���Ũ����ͬ�������Σ�pHԽ��˵���������ˮ��Խ��ǿ�ң���Ӧ����Խ��������HX��HY��HZ��������ǿ������˳��ΪHX��HY��HZ����2����ͬŨ�ȵ�Na2CO3��NaHCO3��Һ��CO32-ˮ��̶ȴ��� HCO3-����0��1 mol��L-1Na2CO3��Һ��pH��0��1 mol��L-1NaHCO3��Һ��pH���ڲ�ͬŨ�ȵ�NH4Cl��Һ��Ũ��ԽС��NH4+ˮ��̶�Խ����ˮ�����Һ������Խ�������Ԣ�0��1 mol��L-1NH4Cl��Һ��pH��0��01 mol��L-1NH4C1��Һ��pH����3����ɸ���ԭ��ء���a��b������aΪ���������a��b��c��d������c������������ӦΪ���������c��d��a��c������cΪ������ a��c��b��c������������c������b�������b>c�����ϣ�a >b>c>d����4�� AlCl3��Һ���ɵõ��������������յõ�����������5�� �Ȼ�����Һ�����ԣ���ΪFe3+ˮ�⣬Fe3++3H2O Fe(OH)3+3H+����6����������Һ����μ���Ba(OH)2��Һ��SO42-�պó�����ȫʱ,�����ķ�Ӧ����Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4��+2H2O���õ�����NaAlO2��Һ����Һ��pH��7��
Fe(OH)3+3H+����6����������Һ����μ���Ba(OH)2��Һ��SO42-�պó�����ȫʱ,�����ķ�Ӧ����Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4��+2H2O���õ�����NaAlO2��Һ����Һ��pH��7��
���㣺���������ˮ���Ӧ�úͽ�����ԱȽϡ�
�����Ѷȣ�����
2������� A��B��C�����ձ��зֱ�ʢ��200mL��ͬ���ʵ���Ũ�ȵ�ϡ���
��1���ֱ�д������װ������Ƭ���淢����Ӧ�����ӷ���ʽ��
A______��B______��?C______��
��2��һ��ʱ���B��Sn��������������Һ��pH______�����������С���������䡱����
��3��һ��ʱ���C�в�����3.36L����״��������ʱ������ǡ��ȫ�������ģ���ԭϡ������Һ�����ʵ���Ũ��Ϊ______mol?L-1��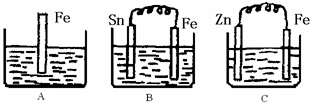
�ο��𰸣���1��A���ǽ������������ܷ����û���Ӧ��ԭ������ʽΪ��Fe+2H+=Fe2++H2����B��Sn��Fe�����ṹ�ɵ�ԭ��أ��������ϻ��ã����������缫��ӦΪ��Fe-2e-=Fe2+��C�У�Zn��Fe�����ṹ�ɵ�ԭ��أ�����п�ϻ��ã������������������������ü������ĵ缫��ӦΪ��2H++2e-=H2�����ʴ�Ϊ��Fe+2H+=Fe2++H2����Fe-2e-=Fe2+��2H++2e-=H2����
��2��B��Sn�������������ĵ缫��ӦΪ��2H++2e-=H2��������������Ũ�ȼ�С�����Լ�����pH���ʴ�Ϊ������
��3��C�����������ĵ缫��ӦΪ��2H++2e-=H2����������3.36L����״������0.15mol����ʱ�����������ӵ����ʵ���Ϊ0.3mol������ԭϡ������Һ�������ӵ����ʵ���Ϊ0.3mol��������������ʵ���0.15mol��c=nV=0.15mol0.2L=0.75mol/L���ʴ�Ϊ��0.75��
���������
�����Ѷȣ���
3��ѡ���� һ��̼����(����)���ε��ԭ��������ͼ���õ�صĵ����Ϊ6mol/L KOH��Һ������˵����ȷ����
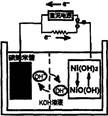
A������H2��̼���ܷŵ�ʱΪ���������ʱΪ����
B�����ʱ������ӦΪNiO(OH)+H2O+e��=Ni(OH)2+OH��
C���ŵ�ʱ����������Һ��pH��С
D���ŵ�ʱ������ӦΪH2+2OH����2e��=2H2O
�ο��𰸣�D
���������A������H2��̼���ܷŵ�ʱΪ���������ʱΪ����������B�����ʱ������ӦΪNi(OH)2- e��+OH��=NiO(OH)+H2O������C���ŵ�ʱ����������Ӧ��NiO(OH)+H2O+e��=Ni(OH)2+OH����c(OH��)����������Һ��pH������D���ŵ�ʱ������ӦΪH2+2OH����2e��=2H2O[����ȷ��
�����Ѷȣ���
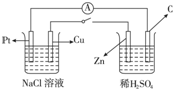
4��ѡ���� ��ͼ�������ձ��õ���������Pt��Cu��Zn��C�ֱ�Ϊ�ĸ��缫�����պϿ��غ�����������ȷ���ǣ�������
A��Cu������OH-Ũ������
B��Cu��Ϊԭ��ظ���
C��������������C������Pt��
D����C������4mol����ת��ʱ��Pt������1molO2����