1、选择题 亚硝酸钠俗称“工业盐”,有很强的毒性,因外观、口感与食盐相似,而常常被误用、误食,为了区分亚硝酸钠与食盐,某研究性小组通过查阅资料后得知:亚硝酸钠具有强氧化性,可与硝酸银溶液反应产生沉淀,亚硝酸是一种弱酸,不稳定,易分解为两种气体,据此设计了如下方案,①分别向盛有两种溶液的试管中加入稀硫酸,如试管中有红棕色气体产生的为亚硝酸钠;②用洁净的玻璃棒分别蘸取两种无色溶液滴在淀粉碘化钾试纸上,出现蓝色的是亚硝酸钠;③向两支盛有硫酸亚铁溶液的试管中分别加入氯化钠和亚硝酸钠,溶液变棕黄色的是亚硝酸钠;④分别向盛有两种溶液的试管中加入硝酸银,有白色沉淀产生的是氯化钠,另一支试管内是亚硝酸钠。其中能够区分亚硝酸钠与食盐的操作及结论正确是(?)
A.①②③④
B.①②④
C.①②③
D.①③④
参考答案:C
本题解析:由题意可知,①可以,加入稀硫酸后,生成亚硝酸,该酸不稳定,易分解为两种气体:NO2、NO;②可以,亚硝酸具有强氧化性,可以把I-氧化为I2;③可以,亚硝酸把Fe2+氧化为Fe3+;④都会生成白色沉淀,无法区别。
本题难度:简单
2、填空题 实验室用图I所示的装置制取干燥的氨气。

(1)A处反应的化学方程式为?。
(2)为收集到干燥的氨气,导管C应接?(填序号)。
(3)装置B中盛装的试剂的名称是?。
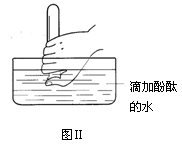
(4)在水槽中加入水(含酚酞),将充满氨气的试管倒置于放入水槽中(如图Ⅱ所示),将拇指稍移开试管口,可观察到的现象为_______________?。
(5)在D、E、F三种气体收集方法中,能用于收集NO的是________(填写序号)。
参考答案:(1)2NH4Cl + Ca(OH)2 2NH3 ↑+ 2H2O + CaCl2?(2)E(3)碱石灰(生石灰或固体氢氧化钠)
2NH3 ↑+ 2H2O + CaCl2?(2)E(3)碱石灰(生石灰或固体氢氧化钠)
(4)溶液进入试管中,无色溶液变红 (5)D
本题解析:(1)A为氨气的发生装置,实验室利用氯化铵和氢氧化钙在加热条件下制取氨气,化学方程式为2NH4Cl + Ca(OH)2 2NH3 ↑+ 2H2O + CaCl2;(2)氨气极易溶于水,不能用排水法收集,氨气的密度比空气小,应用向下排空气法收集,为收集到干燥的氨气,导管C应接E;(3)装置B的作用是干燥氨气,盛装的试剂的名称是碱石灰(生石灰或固体氢氧化钠);(4)氨气极易溶于水,与水反应生成弱碱一水合氨;可观察到的现象为溶液进入试管中,无色溶液变红;(5)NO能与空气中的氧气反应,不能用排空气法收集,一氧化氮不溶于水,可用排水法收集,在D、E、F三种气体收集方法中,能用于收集NO的是D。
2NH3 ↑+ 2H2O + CaCl2;(2)氨气极易溶于水,不能用排水法收集,氨气的密度比空气小,应用向下排空气法收集,为收集到干燥的氨气,导管C应接E;(3)装置B的作用是干燥氨气,盛装的试剂的名称是碱石灰(生石灰或固体氢氧化钠);(4)氨气极易溶于水,与水反应生成弱碱一水合氨;可观察到的现象为溶液进入试管中,无色溶液变红;(5)NO能与空气中的氧气反应,不能用排空气法收集,一氧化氮不溶于水,可用排水法收集,在D、E、F三种气体收集方法中,能用于收集NO的是D。
本题难度:一般
3、选择题 在标准状况下将NO2、NO、O2混合并充满容器,将该容器倒置于水中,气体完全溶解,无气体剩余,若产物也不扩散,则所得溶液的物质的量浓度M,其数值大小范围为……( )
A.0<M<1/22.4
B.1/39.2<M<1/22.4
C.1/39.2<M<1/28
D.1/28<M<1/22.4
参考答案:C
本题解析:本题是有关NO2、NO和O2混合气体溶于水的计算问题,要解决这类问题应抓住两个基本反应及由它们演变出的两个反应(Ⅰ)、(Ⅱ),即:
2NO+O2=2NO2……①
3NO2+H2O=2HNO3+NO……②
②×2+①得:
4NO2+O2+2H2O=4HNO3……(Ⅰ)
①×3+②×2得:
4NO+3O2+2H2O=4HNO3……(Ⅱ)
由(Ⅰ)、(Ⅱ)式中的系数要思考物质的量的变化,确定和寻找有关反应之间量的比例关系,反应物有无过量等等。
混合气体溶于水的气体体积等于所得溶液的体积,且溶液中溶质的物质的量等于溶于水的气体的物质的量,所得溶液的物质的量浓度为(V/22.4)/V =" 1/22.4" (摩/升)
①若混合气体是NO2和O2,且体积比≤4:1,因为发生反应:4NO2+O2+2H2O=4HNO3,生成硝酸的物质的量是溶于水的气体物质的量的4/5,所得溶液的体积等于溶于水的气体体积,所以所得溶液的物质的量浓度为(V/22.4 ×4/5)/V =" 1/28" (摩/升)
若混合气体是NO2和O2,且二者的体积比>4:1,所得溶液的物质的量浓度大于1/28(摩/升)
②若混合气体是NO和O2,且二者体积比≤3:4,因为发生反应:4NO+3O2+2H2O=4HNO3,生成硝酸的物质的量是溶于水的气体物质的量的4/7,所得溶液体积等于溶于水的气体体积,所得溶液的物质的量浓度为(V/22.4 ×4/7)/V = 1/39.2(摩/升)
综合①、②可知,应选择C。
本题难度:一般
4、选择题 据悉,奥运会上使用的发令枪所用的“火药”主要成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学反应方程式为:5KClO3+6P=3P2O5+5KCl,则下列有关叙述错误的是
[? ]
A.上述反应中氧化剂和还原剂的物质的量之比为5:6
B.产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾)
C.上述反应中消耗3molP时,转移电子的物质的量为15mol
D.因红磷和白磷互为同素异形体,上述火药中的红磷可以用白磷代替
参考答案:D
本题解析:
本题难度:简单
5、选择题 室温时,容量为18 mL的试管里充满NO2气体,然后将它倒置于水中,直到管内水面不再上升为止,再通入6 mL O2,最后试管内还有( )?
A.3 mL O2
B.1.5 mL O2?
C.3 mL NO
D.1.5 mL NO?
参考答案:B?
本题解析:18 mL NO2溶于水3NO2~NO,可产生NO为6 mL,再通入6 mL? O2,发生4NO+3O2+2H2O4HNO3,43="6" mLn(O2),n(O2)="4.5" mL,所以余n(O2)="6" mL-4.5 mL="1.5" mL,答案?为B。
本题难度:简单