1������� ����[CO��NH2��2]�����������˹��ϳɵ��л��
��1����ҵ��������CO2��NH3��һ�������ºϳɣ��䷴Ӧ����ʽΪ______��
��2������̼��
=4ʱ��CO2��ת������ʱ��ı仯��ϵ��ͼ1��ʾ��
��A����淴Ӧ����v�棨CO2��______B�������Ӧ����v����CO2��������ڡ���С�ڡ����ڡ�����
��NH3��ƽ��ת����Ϊ______��
��3���˹�����ɲ��ü�ӵ绯ѧ������ȥ��л�����е����أ�ԭ����ͼ2��ʾ��

�ٵ�Դ�ĸ���Ϊ______���A����B������
���������з����ķ�Ӧ����Ϊ______��______��
�۵���������������Һ��pH����ǰ��Ƚ�______�����������ռ�������13.44L����״���������ȥ������Ϊ______g������������ܽ⣩��
�ο��𰸣���1��CO2��NH3�ϳ�CO��NH2��2������Ԫ���غ��֪��ͬʱ����H2O���ɣ���ѧ����ʽΪ��
2NH3+CO2һ������.CO��NH2��2+H2O���ʴ�Ϊ��2NH3+CO2һ������.CO��NH2��2+H2O��
��2������CO2��ת������ʱ��仯ͼ��֪��A��ʱ��Ӧ��δ�ﵽƽ��״̬����Ӧ�Խ�����������У���v�棨CO2��С��B��ƽ��ʱ�Ļ�ѧ��Ӧ���ʣ��ʴ�Ϊ��С�ڣ�
����CO2�ij�ʼ���ʵ���Ϊa����NH3�ij�ʼ���ʵ���Ϊ4a����ͼ��֪��CO2��ת����Ϊ60%����ת���Ķ�����̼Ϊa��60%=0.6a�����ݷ���ʽ��֪��ת����NH3�����ʵ���Ϊ0.6a��2=1.2a����ƽ��ʱ������ת���ʶ�Ϊ1.2a4a��100%=30%��
�ʴ�Ϊ��30%��
��3������ͼ��֪�����ҵ缫����ΪCl2������������Ӧ����AΪ��Դ�����������ҵ�����H2��������ԭ��Ӧ����BΪ��Դ
�ĸ������ʴ�Ϊ��B��
����ͼ��֪�������������������ӷŵ����������������������������ɵ�����������̼��ͬʱ������HCl���������з����ķ�Ӧ����Ϊ��6Cl--6e-�T3Cl2����CO��NH2��2+3Cl2+H2O�TN2+CO2+6HCl��
�ʴ�Ϊ��6Cl--6e-�T3Cl2����CO��NH2��2+3Cl2+H2O�TN2+CO2+6HCl��
��������ӦΪ6H2O+6e-�T6OH-+3H2������6H++6e-�T3H2����
������ӦΪ6Cl--6e-�T3Cl2����CO��NH2��2+3Cl2+H2O�TN2+CO2+6HCl
����������Ӧʽ���Կ��������������ϲ�����OH-��H+����Ŀ��ȣ��������з�Ӧ������H+ͨ�����ӽ���Ĥ������������OH-ǡ�÷�Ӧ����ˮ�������������е��ǰ����Һ��pH���䣻
��������Ӧʽ���Կ�����ת��6mole-ʱ����������3molH2����������1molN2��1molCO2���ʵ���ռ�����13.44L���壬���ʵ���Ϊ13.44L22.4/mol=0.6mol����n��N2��=n��CO2��=0.6mol��15=0.12mol��
���ݷ���ʽCO��NH2��2+3Cl2+H2O�TN2+CO2+6HCl��֪����0.12molN2�����ĵ�CO��NH2��2�����ʵ���ҲΪ0.12mol��������Ϊ��m[CO��NH2��2]=0.12mol��60g?mol-1=7.2g��
�ʴ�Ϊ�����䣬7.2��
���������
�����Ѷȣ�һ��
2��ѡ���� ����N2��g����3H2��g��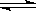 2NH3��g����������Ϊ��Ӧ�ﵽƽ��״̬���ж������ǣ�?��
2NH3��g����������Ϊ��Ӧ�ﵽƽ��״̬���ж������ǣ�?��
A����λʱ��������1molN2��ͬʱ����3molH2
B�������ܱ���������ѹǿ����
C�����ɰ����������백���ֽ���������
D��N2��H2��NH3��Ũ�Ȳ��ٷ����仯
�ο��𰸣�B
������������淴Ӧ�ﵽ��ѧƽ��״̬�ı�־�������淴Ӧ������ȡ������Ũ�ȱ��ֲ��䡣��λʱ��������1molN2��Ϊ�淴Ӧ��ͬʱ����3molH2��Ϊ����Ӧ����v������=v���棩��A��ƽ��״̬����Ӧ�������ʱ�������ʵ�����С�����¡������ܱ������������ѹǿ��С������ѹǿ���䲻��˵����Ӧ�ﵽƽ��״̬����Ӷ���������B�������ɰ����������백���ֽ��������ȼ�v������=v���棩��C��ƽ��״̬�������Ũ�ȱ��ֲ��䣬˵����Ӧ�ﵽƽ��״̬��D��ȷ��
���������⻯ѧƽ��״̬��ֱ�ӱ�־�������淴Ӧ������ȡ������Ũ�ȱ��ֲ��䣩�ͼ�ӱ�־����ϵ��ѹǿ���¶ȡ���ɫ��ƽ��Ħ�������ȣ�����һ��Ҫ���������
�����Ѷȣ�һ��
3��ѡ���� ��Ӧ3A��g��+B��g���T2C��g�������ֲ�ͬ�������½��з�Ӧ����ͬһʱ���ڣ���õķ�Ӧ�����ò�ͬ�����ʱ�ʾΪ����vA�T1mol/L?min?��vC�T0.5mol/L?min?��vB�T0.5mol/L?min����������¸÷�Ӧ���ʴ�С�Ĺ�ϵ��ȷ���ǣ�������
A���ۣ��٣���
B���ۣ��ڣ���
C���٣��ڣ���
D���ڣ��٣���
�ο��𰸣�A
���������
�����Ѷȣ���
4��ѡ���� ��ӦmA(s)��nB(g) pC(g)����H��0����һ���¶��£�ƽ��ʱB���������(B%)��ѹǿ�仯�Ĺ�ϵ��ͼ��ʾ������������һ����ȷ����
pC(g)����H��0����һ���¶��£�ƽ��ʱB���������(B%)��ѹǿ�仯�Ĺ�ϵ��ͼ��ʾ������������һ����ȷ����

��m��n��p��? ��x���ʾ������Ӧ���ʴ����淴Ӧ���� ?��n��p�� ��x���y��ʱ�ķ�Ӧ�����������������¶ȣ��÷�Ӧ��ƽ�ⳣ������
A���٢ڢ�
B��ֻ�Тڢ�
C��ֻ�Т٢�
D���٢ۢ�
�ο��𰸣�B
�����������ӦmA(s)��nB(g) pC(g)����H��0����һ���¶��£���ƽ��ʱB���������(B%)��ѹǿ�仯�Ĺ�ϵ���Կ���������ѹǿ������B�����������������n<p���÷�Ӧ�Ƿ��ȷ�Ӧ�����������¶ȣ�ƽ���������ƶ�������ƽ�ⳣ�����С��X��ʱB��Ũ�ȴ���ƽ��ʱ��Ũ�ȣ�˵����Ӧ�����������ƶ�����������Ӧ�����ʴ����淴Ӧ�����ʡ�X���ѹǿС��y���ѹǿ������x��ķ�Ӧ��������С��y�����ʡ���ѡB��
pC(g)����H��0����һ���¶��£���ƽ��ʱB���������(B%)��ѹǿ�仯�Ĺ�ϵ���Կ���������ѹǿ������B�����������������n<p���÷�Ӧ�Ƿ��ȷ�Ӧ�����������¶ȣ�ƽ���������ƶ�������ƽ�ⳣ�����С��X��ʱB��Ũ�ȴ���ƽ��ʱ��Ũ�ȣ�˵����Ӧ�����������ƶ�����������Ӧ�����ʴ����淴Ӧ�����ʡ�X���ѹǿС��y���ѹǿ������x��ķ�Ӧ��������С��y�����ʡ���ѡB��
�����������ڻ�ѧƽ����й�ͼ�����⣬�ɰ����µķ������з�����
(1)��������ϵ�������ݡ������������������壬������������ԭ���ҹ���
(2)���ۿ��淴Ӧ����������������Ӧ���������Ȼ��Ƿ��ȡ���������Ǽ�С�����䡢�����塢��Һ�����ʲμӻ����ɵȡ�
(3)�������ʵı仯���仯���Ĵ�С����������仯֮����š�
(4)������㡢�յ㡢�յ㣬�������ߵı仯���ơ�
(5)�ȹ���ƽ����ֵ�����磬��ת����һʱ��ͼ�ϣ��ȳ��ֹյ�������ȴﵽƽ�⣬��ʱ���������ɵøñ仯���¶ȸߡ�Ũ�ȴ�ѹǿ�ߡ�
(6)��һ�������ͼ������������ʱ����ȷ��һ�������������������������Ĺ�ϵ
�����Ѷȣ�һ��
5������� 8�֣�һ���¶��£����ݻ�Ϊ1L���ܱ������ڷ���2mol N2O4��8 mol NO2���������·�Ӧ��2NO2������ɫ�� N2O4����ɫ������H<0������Ӧ��NO2��N2O4�����ʵ����淴Ӧʱ��仯����������ͼ��������Ҫ������
N2O4����ɫ������H<0������Ӧ��NO2��N2O4�����ʵ����淴Ӧʱ��仯����������ͼ��������Ҫ������
��1���ڸ��¶��£���Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ��?
��2����t1��10s��t2��20s�������t1��t2ʱ��N2O4��ʾ�ķ�Ӧ���ʣ���������������?mol��L-1��s-1����
��3��ͼ��t1��t2��t3��һ��ʱ�̱�ʾ��Ӧ�Ѿ��ﵽƽ�⣿������������������
��4��t1ʱ������Ӧ������?������������������������淴Ӧ����
��5��ά���������¶Ȳ��䣬����С�������������ƽ����??�ƶ�
�������Ӧ�������淴Ӧ�����ƶ�����
��6��ά��������������䣬�����¶ȣ��ﵽ��ƽ��ʱ��ϵ����ɫ��?��?
������������dz�����䡱��
�ο��𰸣���1��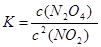 ��2�֣���2��0.1��2�֣���3��t3?��1�֣�
��2�֣���2��0.1��2�֣���3��t3?��1�֣�
��4����?��1�֣���5������ӦӦ����1�֣���6������?��1�֣�
�����������1��ƽ�ⳣ����ָ��һ�������µĿ��淴Ӧ�У�����Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը÷�Ӧ��ƽ�ⳣ������ʽΪ ��
��
��2����t1��t2ʱN2O4�����ʵ���������4mol��3mol��1mol�����Է�Ӧ������1mol��1L��10s��0.1mol/(L��s)��
��3������ͼ���֪��t3ʱ�����ʵ����ʵ������ٷ����仯�����Դ�ʱ��Ӧ�ﵽƽ��״̬��
��4��t1ʱNO2�����ʵ�����С��˵����Ӧ��������Ӧ������еģ�������Ӧ���ʴ����淴Ӧ���ʡ�
��5����Ӧǰ���������С�ģ�������С�ݻ���ѹǿ����ƽ��������Ӧ�����ƶ���
��6������Ӧ�Ƿ��ȷ�Ӧ�����������¶ȣ�ƽ�����淴Ӧ�����ƶ���NO2��Ũ��������ɫ���
�����Ѷȣ�һ��