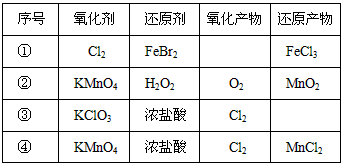
1、选择题 根据下表信息,下列叙述中正确的是
[? ]
A.表中①反应的氧化产物只能有FeCl3
B.表中②生成1mol的O2将有4mol的电子转移
C.表中④的离子方程式配平后,H+的化学计量数为16
D.表中③还原产物是KCl
参考答案:C
本题解析:解析:
A.表中①Fe3+Br_都有可能被氯气所氧化,氧化产物可能有Br2也可能有FeCl3?,故错;
B.表中②生成1mol的O2全由过氧化氢被氧化所得,将有2mol的电子转移,故错
C.表中④的离子方程式配平后为2MnO4-+16H++14Cl-=7Cl2+2Mn2++3H2O,H+的化学计量数为16,故正确;
D.表中③氧化产物和还原产物都是Cl2,故错。
故选:C
本题难度:简单
2、选择题 ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2: 2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O?下列说法正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O?下列说法正确的是( )
A.KClO3在反应中得到电子
B.ClO2是氧化产物
C.H2C2O4在反应中被还原
D.1 mol KClO3参加反应有2 mol电子转移
参考答案:A
本题解析:由反应可知,KClO3为氧化剂,在反应中得到电子,因此A正确。而ClO2是还原产物,故B错误。H2C2O4在反应中被氧化,故C错误。由方程式可知,2mol KClO3参加反应有2 mol电子转移,因此1 mol KClO3参加反应有1mol电子转 移,故D错误。综上,答案选A。
点评:氧化还原反应是必修一的重点内容,尤其是对氧化还原反应的应用,更是高考的重要考点。对氧化还原反应的掌握,应注意从其化合价以及电子转移入手,可达到事半功倍的效果。
本题难度:简单
3、填空题 某反应中反应物与生成物有: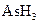 、
、 、
、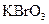 、
、 、
、 、
、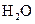 和一种未知物质X。
和一种未知物质X。

 (1)已知
(1)已知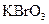 在反应中得到电子,则该反应的还原剂是?。
在反应中得到电子,则该反应的还原剂是?。
 (2)已知0.2mol
(2)已知0.2mol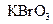 在反应中得到1mol电子生成X,则X的化学式为?。
在反应中得到1mol电子生成X,则X的化学式为?。
 (3)根据上述反应可推知?。
(3)根据上述反应可推知?。
 ? a.氧化性:
? a.氧化性: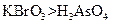 ? b.氧化性:
? b.氧化性: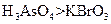
 ? c.还原性:
? c.还原性: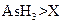 ? d.还原性:
? d.还原性: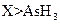
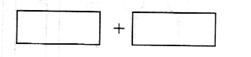
 (4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方
 向和数目:
向和数目:
参考答案:
 (1)AsH3
(1)AsH3
 (2)Br2
(2)Br2
 (3)ac
(3)ac
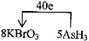
 (4)?
(4)?
本题解析:(1)KBrO3在反应中得到电子,则另外一种化合价变化的元素在反应中失去电子被氧化,所给物质中As元素化合价发生了变化,低价态的AsH3是还原剂。
(2)0.2mol KBrO3得到1mol电子,说明Br元素在反应中降低了5价,所以x的化学式为Br2。
(4)利用氧化还原反应中电子得失相等的规律可配平该方程式为
8KBrO3+5AsH3+4H2SO4===4K2SO4+4Br2+5H3AsO4+4H2O
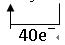

本题难度:一般
4、选择题 24 mL 0.05 mol・L-1的 Na2SO3溶液恰好与20 mL 0.02 mol・L-1的K2R2O7的溶液完全反应,则R元素在还原产物中的化合价为
0.02 mol・L-1的K2R2O7的溶液完全反应,则R元素在还原产物中的化合价为
A.0
B.+2
C.+3
D.+6
参考答案:C
本题解析:略
本题难度:简单
5、推断题 (12分)按图所示实验过程填空:
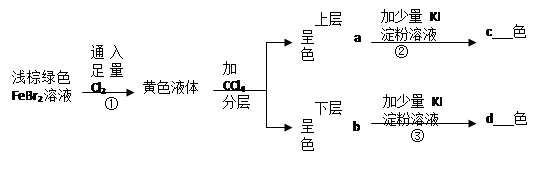
(1)写出上述反应的离子方程式:
①?②?③?
(2)填空:
a??b ??c??d??
参考答案:(1)① 2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2?(2分)
② 2Fe3++2I-=2Fe2++I2?(3分)?③ Br2+2I-=2Br-+I2?(3分)
(2)? a 棕黄? b 橙红? c蓝? d 蓝色?(各1分)
本题解析:①发生的反应为:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2,所得的黄色液体为溴水。加CCl4后分层,上层为FeCl3溶液,呈棕黄色;下层为溴的CCl4溶液,呈橙红色;②发生的反应为:2Fe3++2I-=2Fe2++I2,反应后所得的溶液的溶质为I2,I2遇淀粉变蓝色。③发生的反应为:Br2+2I-=2Br-+I2,淀粉遇碘变蓝色。
点评:此题考查卤素单质之间的相互转换,属于基础题。对于卤素单质,应特别注意其颜色。
本题难度:一般