1、选择题 能够充分说明在恒温下的密闭容器中,反应2SO2+O2=2SO3已达平衡状态的标志是
A.容器中SO2、O2、SO3的物质的量之比为2:1:2
B.SO2和SO3的物质的量浓度相等
C.单位时间内生成2molSO3时,即消耗1molO2
D.反应容器内压强不随时间变化而变化
参考答案:D
本题解析:略
本题难度:简单
2、选择题 在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)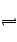 CO(g)+H2O(g)
CO(g)+H2O(g)
△H=aKJ・mol-1,其化学平衡常数K和温度t的关系如下表:
t/℃
| 700
| 800
| 830
| 1000
| 1200
|
K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
下列说法中正确的是
A.该反应的正反应为吸热反应,即a>0
B.当υ正(H2)=υ正(H2O )时,该反应达到化学平衡状态
C.当其他条件不变时,若缩小容器的体积,则有利于该反应平衡正向移动
D.当平衡浓度符合c(CO2)・c(H2)=c(CO)・c(H2O)时的温度为830℃、、
参考答案:
本题解析:AD根据表中数据可知,随着温度的升高K值是增大,这说明升高温度平衡向正反应方向移动,因此正方应是吸热反应,A正确;B中反应速率的方向是相同的,速率之比是相应的化学计量数之比,因此B中的关系始终是成立,不正确。该反应是体积不变的可逆反应,改变压强平衡不移动,C不正确;根据平衡常数的表达式可知,如果c(CO2)・c(H2)=c(CO)・c(H2O),则此时K=1,所以选项D正确,答案选AD。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生基础知识的巩固与训练,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:简单
3、选择题 可逆反应aX(g)+bY(g) cZ(g)在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)-时间(t)图像如图。下列说法正确的是(? )
cZ(g)在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)-时间(t)图像如图。下列说法正确的是(? )

A.若a+b=c,则t0时只能是增大反应体系的压强
B.若a+b=c,则t0时只能是加入催化剂
C.若a+b≠c,则t0时只能是加入催化剂
D.若a+b≠c,则t0时只能是增大体系的压强
参考答案:C
本题解析:若a+b=c,则该反应是个反应前后气体体积相等的可逆反应。在t0时改变条件后由于V正=V逆。所以化学反应速率加快但是平衡不发生移动。改变的条件可能是增大反应体系的压强,也可能是加入催化剂。A.B都错误。若a+b≠c,则该反应是个反应前后气体体积不等的可逆反应。在t0时改变条件后由于V正=V逆。所以化学反应速率加快但是平衡不发生移动。改变的条件t0时只能是加入催化剂。C正确,D错误。
本题难度:一般
4、选择题 下列叙述中可以说明反应2HI(g)  H2(g)+I2(g)已达平衡状态的是
H2(g)+I2(g)已达平衡状态的是
①单位时间内生成n mol H2的同时生成n mol HI?②一个H―H键断裂的同时有两个H―I键断裂?③百分组成HI%=I2%?④反应速率v(H2)=v(I2)=1/2v(HI)?⑤[HI]∶[H2]∶[I2]=2∶1∶1?⑥v(HI)分解=v(HI)生成?⑦压强不变
A.①③⑤
B.②⑥
C.④⑤
D.④⑥⑦
参考答案:B
本题解析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以选项⑥可以说明。①中反应速率的方向相反,但不能满足速率之比是相应的化学计量数之比,不能说明。②中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,可以说明。平衡时各种物质的浓度不再发生变化,但各种的浓度之间不一定满足某种关系,③⑤不能说明。速率之比是相应的化学计量数之比,因此④中的关系始终是成立,不能说明。根据反应的方程式可知,反应前后体积是不变的,因此压强始终是不变的,所以⑦不能说明,因此答案选B。
点评:该题是中等难度的试题,也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确平衡状态的特点,然后结合具体的可逆反应灵活运用即可。
本题难度:简单
5、选择题 可逆反应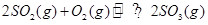 ,从正方向开始,并达到了平衡。此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是?
,从正方向开始,并达到了平衡。此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是?
A.新平衡体系中,SO2和O2物质的量之比仍为2∶1
B.平衡向正反应方向移动了,原因是正反应速率增大了,逆反应速率减小了
C.新平衡体系与旧平衡体系比较,SO3的浓度肯定增大了
D.若所采取的措施是缩小容器的容积,则新平衡SO2和O2转化率之比和旧平衡中SO2和O2的转化率之比都是1∶1
参考答案:A
本题解析:
A项,SO2和O2减少的物质的量之比为2∶1,所以新平衡体系中,SO2和O2物质的量之比仍为2∶1,故A正确;B项,逆反应速率也可能增加,只是比正反应速率增加的少,错误;C项,把SO3移走一些,可以导致SO2和O2又消耗了一些,并再次达到平衡,此时SO3的浓度减少,错误;D项若所采取的措施是缩小容器的容积,平衡向正反应方向移动,SO2和O2转化率增大,之比大于1,错误。
本题难度:一般