1、填空题 锌锰废电池经处理后,生产并回收硫酸锌及碳酸锰,其中生产工业级碳酸锰工艺如下:
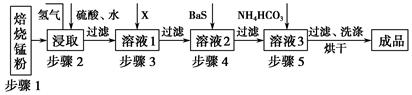
试回答下列问题:
(1)锰在元素周期表中位于第________周期,第________族。
(2)步骤1和步骤2是将MnO2转化为MnO并溶于硫酸,其中步骤2中的氢气,是另一个流程产生的副产品,请写出产生氢气的反应方程式__________________________。
(3)步骤3和步骤4都是除杂质。
①X是一种“绿色”氧化剂,则X是________(填化学式)。
②步骤3是除去杂质Fe2+。请用文字和必要的方程式简述除去Fe2+的方法(已知三种离子沉淀的pH范围为Fe3+:2.7~3.7,Mn2+:8.6~10.1,Fe2+:7.6~9.6)_________________________________________________________。
③步骤4中主要反应方程式为:MeSO4+BaS=MeS↓+BaSO4↓(Me主要为Pb、Cd、Hg等),则其除去杂质的原理是_________________________________________________。
(4)已知进行步骤5的操作时,溶液3(主要成分为MnSO4)会产生大量无色无味的气泡,则步骤5反应的化学方程式为_______________________________________。
参考答案:(1)四 ⅦB
(2)Zn+H2SO4=ZnSO4+H2↑
(3)①H2O2 ②在酸性条件下加入双氧水,将Fe2+氧化成Fe3+、2Fe2++H2O2+2H+=2Fe3++2H2O,调节pH至3.7~8.6,使Fe3+沉淀完全,Fe3++3H2O?Fe(OH)3+3H+ ③以BaS为沉淀剂,使Pb2+、Cd2+、Hg+等金属离子,生成更难溶的硫化物而除去
(4)MnSO4+2NH4HCO3=(NH4)2SO4+MnCO3↓+H2O+CO2↑
本题解析:(2)废电池回收硫酸锌和碳酸锰,故另一个工艺是制取硫酸锌,锌皮与稀硫酸反应生成氢气:Zn+H2SO4=ZnSO4+H2↑
(3)①具有强氧化性的“绿色”氧化剂,显然是H2O2,它的加入也不会引入新的杂质。②由题给的三种离子沉淀pH可知,为除去Fe2+、Fe3+,应将Fe2+先氧化为Fe3+,然后调节溶液的pH在3.7~8.6之间,以便除净Fe3+而不损失Mn2+。③难溶电解质有生成更难溶电解质的趋势,故利用沉淀的转化实现了除去Pb2+、Cd2+、Hg+。
(4)根据气体是无色无味,可知该气体是CO2,故该反应的化学方程式为MnSO4+2NH4HCO3=(NH4)2SO4+MnCO3↓+CO2↑+H2O。
本题难度:一般
2、填空题 钛合金是航天航空工业的重要材料。由钛铁矿(主要成分为钛酸亚铁,化学式为FeTiO3)制备Ti等产品的一种工艺流程示意图如下:

已知:① TiO2+易水解,只能存在于强酸性溶液中。 ②常温下,难溶电解质溶解度与pH关系图。
③25 ℃时TiO(OH)2溶度积Ksp=1×10-29

回答下列问题:
(1)写出钛铁矿酸浸时,反应的离子方程式?。
(2)操作Ⅱ包含的具体操作方法有?。
(3)向“富含TiO2+溶液”中加入Na2CO3粉末的作用是?, TiO2+水解的离子方程式为?,当溶液pH= ?时,TiO(OH)2已沉淀完全。
(4)加入铁屑将Fe3+转化为Fe2+的原因是?。
参考答案:(1)FeTiO3+4H+ = TiO2++Fe2++2H2O
(2)蒸发浓缩,冷却结晶,过滤
(3)调节溶液pH,促进TiO2+水解? TiO2++2H2O TiO(OH)2+2H+?2
TiO(OH)2+2H+?2
(4)避免使Fe3+和TiO2+共沉淀。
本题解析:(1)钛铁矿酸浸时,发生反应的化学方程式为FeTiO3+2H2SO4= TiOSO4+FeSO4+2H2O,其相应的离子方程式FeTiO3+4H+ = TiO2++Fe2++2H2O。(2)向含有TiO2+、Fe2+、Fe3+等的酸性溶液中加入适量的Fe粉,发生反应:2Fe3++Fe=3Fe2+.然后将溶液蒸发浓缩、冷却结晶就会产生FeSO4・7H2O.然后将晶体过滤出来。就得到了绿矾。旅游热中含有大量的TiO2+离子,向该溶液中加入Na2CO3粉末,调整溶液的酸碱性,促进TiO2+水解,发生反应TiO2++2H2O TiO(OH)2+2H+。由图像可知当溶液的PH=2时TiO(OH)2已沉淀完全。(4)若不加入Fe粉,就会同时产生TiO(OH)2和Fe(OH)3.导致制取的物质纯度不高。所以加入铁屑将Fe3+转化为Fe2+避免使Fe3+和TiO2+共沉淀。
TiO(OH)2+2H+。由图像可知当溶液的PH=2时TiO(OH)2已沉淀完全。(4)若不加入Fe粉,就会同时产生TiO(OH)2和Fe(OH)3.导致制取的物质纯度不高。所以加入铁屑将Fe3+转化为Fe2+避免使Fe3+和TiO2+共沉淀。
本题难度:一般
3、选择题 下列不属于复合材料的性能的是
[? ]
A.强度高
B.密度大
C.耐高温
D.耐腐蚀
参考答案:B
本题解析:
本题难度:简单
4、选择题 工业上生产水泥和玻璃都用到的一种原料是?
[? ]
A.石英
B.纯碱
C.石灰石
D.黏土
参考答案:C
本题解析:
本题难度:简单
5、选择题 从2009年的哥本哈根,到2010年的两会的召开和上海世博会,“低碳经济”已成为新的时尚流行全球。“低碳经济”是指低能耗、低污染、低排放为基础的经济模式。下列做法不符合“低碳经济”的是?(?)
A.利用太阳能、风能和氢能等新能源代替化石燃料
B.大力开发丰富的煤炭资源,减少对石油的 依赖
依赖
C.在生产和生活中提倡使用节能技术和节能用具
D.一些国家世博馆的外壳使用非晶硅薄膜或复合材料,以充分利用太阳能
参考答案:B
本题解析:略
本题难度:简单