1、选择题 由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH =1,c(Al3+)=0.4 mol・L-1,c(SO42-)=0.8 mol・L-1,, 则c(K+)为
[? ]
A. 0.15 mol・L-1
B. 0.2 mol・L-1
C. 0.3 mol・L-1
D. 0.4 mol・L-1
2、选择题 向MgCl2、AlCl3的混合溶液开始滴加6mol/L的试剂A,之后改滴试剂B,所得沉淀物质的量Y(mol)与试剂体积V(mL)间的关系如图所示。以下结论不正确的是(?)
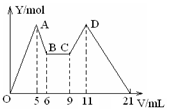
A.从6到9,相应离子反应方程式为H++OH-=H2O
B.A 是NaOH,B是盐酸,且c(NaOH):c( HCl) = 2:1
C.原混合液中,c(Al3+):c(Mg2+):c(Cl-) = 1:1:5
D.A是盐酸,B是NaOH, 且c(NaOH) =" 2c" (HCl)
3、填空题 (6分)某学生为了测定由两种元素形成的气态化合物X的组成,进行了如图所示的实验,将装置内空气排尽后,把气体X由注射器A缓慢送入装有CuO的B装置,使之完全反应(气态化合物X与CuO均无剩余),得到如下结果:
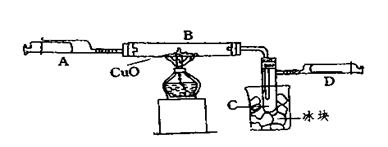
①实验前B管及药品的质量为21.32克,实验后为21.16克
②C管中收集到的物质电解后可得到H2和O2,在D中收集到的是N2。
③X中两元素的质量比是14:3。问:
(1)C中收集到的液体,物质的量是 mol;
(2)在实验中看到的现象是 。
(3)B中反应的化学方程式是 。
4、选择题 阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是
A.0.25molNa2O2中含有的阴离子数为0.5×6.02×1023
B.7.5gSiO2晶体中含有的硅氧键数为0.5×6.02×1023
C.2.24LCH4中含有的原子数为0.5×6.02×1023
D.250mL2mol/L的氨水中含有NH3・H2O的分子数为0.5×6.02×1023
5、选择题 下列溶液中的氯离子浓度与50 mL 1 mol・L-1的AlCl3溶液中氯离子浓度相等的是( )
A.150 mL 1 mol・L-1的NaCl
B.75 mL 2 mol・L-1的NH4Cl
C.150 mL 3 mol・L-1的KCl
D.75 mL 2 mol・L-1的CaCl2