1、填空题 在其他条件不变时,增大反应物浓度,反应速率?(填加快、不变或减慢,下同) ,降低温度,反应速率?;使用正催化剂(简称催化剂)可以?反应速率;有固体参加的反应,增大固体的表面积,反应速率??。
参考答案:加快;减慢;加快;加快
本题解析:考查外界条件对反应速率的影响。在其它条件不变时,增大浓度或升高温度或使用催化剂或增大反应物的接触面积,反应速率就增大。
本题难度:一般
2、填空题 在锌与盐酸反应的实验中,一个学生得到的结果如下表所示:
?
| 锌的质量/g
| 锌的形状
| 温度/℃
| 溶解于酸所花的时间/s
|
A
| 2
| 薄片
| 5
| 400
|
B
| 2
| 薄片
| 15
| 200
|
C
| 2
| 薄片
| 25
| 100
|
D
| 2
| 薄片
| 35
| 50
|
E
| 2
| 薄片
| 45
| 25
|
F
| 2
| 粉末
| 15
| 5
|
试求:
(1)画一幅以时间对温度的曲线图(纵轴表示时间,横轴表示温度).
(2)利用所画的曲线图,关于温度影响反应速率你能得出什么结论?
(3)20℃时,2g锌箔溶解于酸中需花多少时间?
(4)对比结果B与F,解释F为什么那么快?
参考答案:详见解析
本题解析:
(1)如下图所示
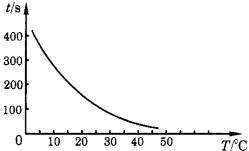
(2)对于该溶液,温度每升高10℃,反应速率加快到原来的2倍。
(3)约150s。
(4)这是因为B中锌是块状,F中锌是粉末状,粉末状与酸溶液的接触面积要比块状大得多,从而使有效碰撞次数大大增多,加快了反应速率。
本题难度:简单
3、选择题 右图曲线a表示放热反应? X(g) + Y(g)  ?Z(g) + M(g) + N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
?Z(g) + M(g) + N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是

A.升高温度
B.加大X的投入量
C.加催化剂
D.增大体积
参考答案:C
本题解析:由图象可知,由曲线a到曲线b,到达平衡的时间缩短,改变条件,反应速率加快,且平衡时x的转化率不变,说明条件改变不影响平衡状态的移动,该反应正反应是放热反应,升高温度,反应速率加快,平衡向逆反应移动,x的转化率降低,故A错误;加大X的投入量,X浓度增大,反应速率加快,平衡向正反应移动,但x的转化率降低,故B错误;加入催化剂,反应速率加快,催化剂不影响平衡移动,x的转化率不变,故C正确;增大体积,压强减小,该反应前后气体的物质的量不变,压强降低平衡不移动,但反应速率降低,故D错误,所以本题的答案选择C。
点评:本题考查了平衡的移动,该考点是高考考查的重点,本题要抓住的是X的转化率不变且达到平衡的时间缩短,例如若选项中如果增大压强也可以选择,该题难度中等。
本题难度:一般
4、选择题 假设C+CO2

2CO(正反应为吸热反应)的反应速率是v1,反应N2+3H2

2NH3(正反应为放热反应)的速率v2,当同时升高两反应的温度时,v1和v2的变化情况为( )
A.v1减v2增
B.同时增大
C.同时减少
D.v1增v2减
参考答案:化学反应无论是吸热反应还是放热反应,温度升高,活化分子的百分含量增大,有效碰撞的次数增大,化学反应速率都增大.
故选B.
本题解析:
本题难度:一般
5、填空题 (8分)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示。回答下列问题:
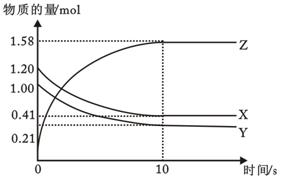
(1)反应开始到10s,用Z表示的反应速率为 ;
(2)反应开始到10s,X的物质的量浓度减少了 ;
(3)反应开始到10s时,Y的转化率为 ;
(4)反应的化学方程式为 。
参考答案:
(1)0.079mol/(L・s) (2)0.395mol/L (3)79% (4)X+Y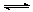 2Z
2Z
本题解析:略
本题难度:简单