1、选择题 用1L?1mol?L-1NaOH溶液吸收0.9molCO2,所得溶液中的CO32-和HCO3-的物质的量浓度之比是
A.5:4
B.4:5
C.1:8
D.8:1
参考答案:C
本题解析:分析:用1L?1mol?L-1NaOH溶液吸收0.9molCO2,所得产物有Na2CO3和NaHCO3,根据Na元素和C元素守恒列式计算.
解答:用1L?1mol?L-1NaOH溶液吸收0.9molCO2,所得产物有Na2CO3和NaHCO3,
设生成xmolNa2CO3,ymolNaHCO3,
则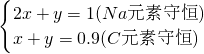
解之得:
所得溶液中的CO32-和HCO3-的物质的量浓度之比等于物质的量之比,为0.1:08=1:8,
故选C.
点评:本题考查物质的量浓度的计算,题目难度不大,注意从质量守恒的角度分析.
本题难度:简单
2、选择题 下列表格中各项都正确的一组是
A.A
B.B
C.C
D.D
参考答案:A
本题解析:分析:溶液中电离出的阴离子全部是氢氧根离子的化合物为碱;
金属阳离子和酸根阴离子构成的化合物为盐;
水溶液中或熔融状态下能导电的化合物为电解质;
水溶液中和熔融状态下都不能导电的化合物为非电解质.
解答:A、各物质符合物质类别概念,故A正确;
B、纯碱是碳酸钠属于盐类,铁是单质不是非电解质,故B错误;
C、明矾是硫酸铝钾属于盐,石墨是单质不是电解质,醋酸是弱电解质,故C错误;
D、NaClO是盐,溶于水全部电离,属于强电解质,故D错误;
故选A.
点评:本题考查了酸碱盐、电解质、非电解质概念的理解和分析判断,熟练掌握物质组成和性质是解题关键,题目较简单.
本题难度:一般
3、选择题 100℃时,KCl溶液中溶质的物质的量浓度为C1.降至室温后析出m?g?KCl晶体(晶体中不含结晶水),所得溶液中溶质的物质的量浓度为C2,则下列说法不正确的是
A.一定条件下,KCl的溶解度是有限的
B.溶液中KCl的物质的量浓度C1一定大于C2
C.降温前后,溶液中KCl的物质的量未发生改变
D.降温过程中,结晶和溶解的速率可能出现相等
参考答案:C
本题解析:分析:溶液中固体的溶解和结晶为可逆过程,降至室温后析出mgKCl晶体,说明随着温度的降低,溶解度降低,由于溶液体积不变,则溶液的质量分数,物质的量浓度都减小,以此解答该题.
解答:A.不同温度下,KCl的溶解度不同,且溶剂不同,溶解度也不同,故A正确;
B.降至室温后析出mgKCl晶体,由于溶液体积不变,物质的量浓度减小,故B正确;
C.降至室温后析出mgKCl晶体,溶液中KCl的物质的量分数改变,故C错误;
D.溶液中固体的溶解和结晶为可逆过程,当达到平衡时,结晶和溶解的速率相等,故D正确.
故选C.
点评:本题考查溶液的物质的量浓度大比较、溶解度等问题,题目难度不大,注意把握饱和溶液的特点以及影响溶解平衡的因素.
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数的值.下列叙述正确的是
A.1?L?0.1?mol?L-1?NH4Cl溶液中,NH4+的数目为0.1NA
B.标准状况下,11.2?L的Cl2溶于水,转移的电子总数为0.5NA
C.14?g乙烯、丙烯的混合气体,含有C一H键数为2NA
D.标准状况下,2.24?LCH2Cl2中含有C1原子数为0.2NA
参考答案:C
本题解析:分析:A.铵根离子发生水解;
B.Cl2与水的反应是可逆反应;
C.依据乙烯和丙烯的最简式相同,计算分析判断;
D.标准状况下,CH2Cl2是液体.
解答:A.铵根离子发生水解,NH4+的数目小于0.1NA,故A错误;
B.Cl2与水的反应是可逆反应,可逆反应不能进行到底,转移的电子总数小于0.5NA,故B错误;
C.乙烯和丙烯最简式相同,14g由乙烯和丙烯最简式CH2的物质的量为1mol,含有C一H键数为2NA,故C正确;
D.标准状况下,CH2Cl2是液体,2.24?LCH2Cl2的物质的量不是0.1mol,故D错误.
故选C.
点评:本题考查阿伏加德罗常数,题目难度不大,注意从物质的组成、结构、性质、聚集状态以及存在的条件是否标准状况等角度思考.
本题难度:一般
5、选择题 下列有关溶液的说法中,正确的是
A.含H+的溶液显酸性,含OH-的溶液显碱性
B.用丁达尔现象实验可区分葡萄糖溶液和氢氧化铁胶体
C.某饱和溶液变成不饱和溶液,溶质的质量分数一定减小
D.标准状况下,2.24?L?NH3溶于水制得1L氨水,则c?(NH3?H2O)=0.1mol?L-1
参考答案:B
本题解析:分析:A.溶液的酸碱性取决于溶液中氢离子浓度与氢氧根离子浓度的相对大小;
B.胶体有丁达尔效应;
C.在不指明温度的情况下饱和与不饱和溶液溶质质量分数无法比较;
D.NH3?H2O是弱电解质.
解答:A.判断溶液的酸碱性应根据溶液中氢离子浓度与氢氧根离子浓度的相对大小判断,故A错误;
B.溶液无丁达尔效应,胶体有丁达尔效应,可用丁达尔效应可以区别溶液与胶体,故B正确;
C.在不指明温度的情况下饱和与不饱和溶液溶质质量分数无法比较大小,相同温度饱和溶液一定比不饱和溶液质量分数要大,故C错误;
D.NH3?H2O是弱电解质,能发生部分电离,浓度小于0.1mol?L-1,故D错误.
故选B.
点评:本题考查酸碱的定义、胶体的性质、饱和溶液、弱电解质的电离等,难度不大,注意溶液的酸碱性取决于溶液中氢离子浓度与氢氧根离子浓度的相对大小.
本题难度:一般