1、选择题 新制氯水与久置的氯水相比较,下列结论正确的是(? )
A.颜色相同
B.都能使有色布条褪色
C.都含有HClO
D.加AgNO3溶液都能生成白色沉淀
参考答案:D
本题解析:新制氯水中含有氯气和次氯酸,具有强氧化性和漂泊性,溶液显淡黄绿色。氯水久置后,将变为稀盐酸,失去漂泊性,但酸性增强,溶液是无色,所以正确的答案选D。
点评:该题是基础性试题的考查,试题注重基础,兼顾能力。该题的关键是掌握次氯酸的性质,进而得出氯水久置后的变化,难度不大,学生不难得分。
本题难度:一般
2、实验题 (15分)下图是一套制取并验证氯 气部分化学性质的实验装置。
气部分化学性质的实验装置。
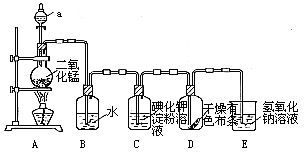
反应的方程式:MnO2+4HCl(浓) MnCl2+2H2O+ Cl2↑回答下列问题:
MnCl2+2H2O+ Cl2↑回答下列问题:
(1)上述反应中氧化剂是____?,还原剂是__?__。
(2)当Cl2气流通过一段时间后,装置B中溶液的pH值____7(填“>”“<”或“=”),写出Cl2与水反应的方程式?.??
(3)当有少量Cl2气流通过后,观察到装置C中的溶液变为_?___色,反应的离子方程式为?_,这个实验证明氯气的氧化性比碘单质?_?___(填“强”或“弱”).
(4)当Cl2气流持续通过时装置D中干燥的有色布条能否褪色?为什么?
?。
(5)装置E的作用是__?_。
(6)制取标况下氯气4.48升,至少需要MnO2?克。(Mn-55,O-16)
参考答案:(1) _MnO21分, _?HCl1分_。(2) __<?略2分
(3)略? 2分?强_?1分_.
(4)?不能?略? 2分。
(5)吸收尾气? 2分_。
(6)17.4 2分
本题解析:略
本题难度:一般
3、选择题 关于氯水的叙述正确的是
A.新制氯水可使红色石蕊试纸先变蓝后褪色
B. 氯水中只含氯分子
氯水中只含氯分子
C.光照氯水有气泡产生,该气体是Cl2
D.氯水放置数 天后,几乎无漂白性
天后,几乎无漂白性
参考答案:D
本题解析:略
本题难度:一般
4、填空题 研究CO、SO2、NO等大气污染气体的综合处理与利用具有重要意义。
(1)以CO或CO2与H2为原料,在一定条件下均可合成甲醇,你认为用哪种合成设计线路更符合“绿色化学”理念:(用化学反应方程式表示)?。
(2)如图所示是用于合成甲醇产品中甲醇含量的检测仪。写出该仪器工作时的电极反应式:
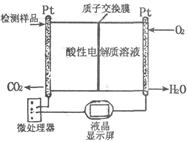
负极?,正极?。
(3)一定条件下,NO2和SO2反应生成SO3(g)和NO两种气体,现将体积比为1:2的NO2和SO2的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是?。(填序号)
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3、NO的体积比保持不变
D.每消耗 1 mol SO2,同时生成1 mol NO