1、选择题 下列有关物质的性质和该性质的应用均正确的是
A.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀
B.二氧化硅不与任何酸反应,可用石英制造耐酸容器
C.常温下浓硫酸能与铝发生钝化,可在常温下用铝制贮藏贮运浓硫酸
D.二氧化氯具有还原性,可用于自来水的杀菌消毒
2、实验题 二氧化锰(MnO2)与浓盐酸混合加热可得到氯气、氯化锰等,下图是制取并探究Cl2化学性质的装置图。

(1)写出圆底烧瓶中反应的化学方程式?。
(2)A中m管的作用是?;装置F的作用是?。
(3)若要得到干燥纯净的气体,则B中应盛放的试剂是??,C中应盛放的试剂是? ?。
?。
(4)E中若装有FeCl2溶液,反应的离子方程式为?;E中若装有淀粉碘化钾溶液,能观察到的实验现象是?。
(5)实验中发现:浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气。针对上述现象,化学小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通人HCl气体,加热
 ? b.稀盐酸滴人MnO2中,然后加入NaCl固体,加热
? b.稀盐酸滴人MnO2中,然后加入NaCl固体,加热
c.稀盐酸滴入MnO2中,然后加入浓硫酸,加热
d.MnO2与NaCl的浓溶液混合,加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是?;实验c的目的是?。
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是?。
3、选择题 下列对氯气的说法不正确的是( )
A.氯气是由舍勒发现的
B.干燥的氯气不能使有色布条褪色
C.氯气不能支持燃烧
D.用氯气消毒自来水不如用臭氧消毒自来水好
4、选择题 将过量的氯气通入30mL浓度为10.0mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3的共存体系。下列判断正确的是
A.与NaOH反应的氯气一定为0.15 mol
B.当反应中被氧化的氯元素和被还原的氯元素之比为1:4时,溶液中NaClO和NaClO3的物质的量之比为3:1
C.溶液中n(Na+):n(Cl-)可能为7:3
D.若Cl2与NaOH的反应中转移的电子为n mol,则0.15<n<0.35
5、选择题 将一定量的 通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中
通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中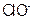 和
和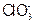 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是
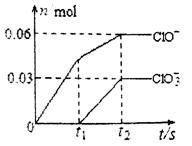
A.苛性钾溶液中KOH的质量是4.94g
B.反应中转移电子的物质的量是0.21mol
C.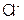 的物质的量为0.09mol
的物质的量为0.09mol
D.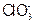 的生成是由于KOH过量引起的
的生成是由于KOH过量引起的