1、选择题 .某元素最高正价与负价的绝对值之差为4,该元素的离子与跟其核外电子排布相同的离子形成的化合物是
A.K2S
B.MgO
C.MgS
D.NaF
2、选择题 氮化钠和氢化钠与水反应的化学方程式如下:Na3N + 3H2O=3NaOH + NH3,NaH + H2O=NaOH + H2↑。有关Na3N和NaH的叙述正确的是
A.离子半径:Na+>N3->H+
B.与水反应都是氧化还原反应
C.与盐酸反应都只生成一种盐
D.加热熔化时,都只破坏离子键
3、填空题 己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大。X与N同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y原子的L层电子数是K层电子数的2倍;U原子的最外层电子数是其电子层数的2倍,试回答下列问题:
(1)YW2的电子式?;Z的氢化物结构式为?;写出U元素在周期表中的位置?。
(2)原子半径:U?V(填>、<或=,下同);气态氢化物的水溶液的酸性:U?V。
(3)写出UW2与V元素的单质在水溶液中反应的化学方程式是?。
(4)由X、Z组成的一种化合物化学式为ZX5,其各原子均达到同周期稀有气体原子的稳定结构,该物质属于?(填“离子”或“共价”)化合物。
(5)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量氢氧化钠溶液在加热条件下反应的离子方程式为:?。
4、填空题 (15分) 已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E。又知A原子的p轨道为半充满,其形成的简单氢化物的沸点是同主族非金属元素的氢化物中最高的。D原子得到一个电子后其3p轨道将全充满。B+离子比D原子形成的离子少一个电子层。C与B可形成BC型的离子化合物。E的原子序数为29。
请回答下列问题:
(1) 元素A简单氢化物中A原子的杂化类型是?,B、C、D的电负性由小到大的顺序为
__?(用所对应的元素符号表示)。C的气态氢化物易溶于水的原因是?。
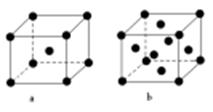
(2)E原子的基态电子排布式为?。元素E的单质晶体在不同温度下可有两种堆积方式,晶胞分别如右图a和b所示,则其面心立方堆积的晶胞与体心立方堆积的晶胞中实际含有的E原子的个数之比为?。
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
离子晶体
| NaCl
| KCl
| CaO
|
晶格能/kJ・mol-1
| 786
| 715
| 3401
|
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:?。
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是?。
5、选择题 下列各组粒子具有相同的质子数和电子数的是(?)
A.OH-、H2O、F-
B.NH3、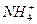 、
、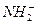
C.H3O+、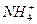 、
、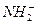
D.HCl、F2、H2S