1������� ��1������ƽ�����ʢ��ǿ��ԭ��Һ̬�£�N2H4����ǿ������Һ̬˫��ˮ������0��4molҺ̬�º�0��8mol H2O2��Ϸ�Ӧ�����ɵ�����ˮ�������ų�256��7kJ������(25�桢101 kPa�²�õ�����)��
�ٷ�Ӧ���Ȼ�ѧ����ʽΪ__________________________��
������֪H2O(l)��H2O(g) ��H��+44kJ/mol����16gҺ̬����Һ̬˫��ˮ��Ӧ����Һ̬ˮʱ�ų���������
__________________________��
�۴˷�Ӧ���ڻ���ƽ������ͷŴ����ȺͿ��ٲ������������⣬����һ���ܴ���ŵ���__________________________��
��2����ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̡���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�����������֪��N��N���ļ�����948��9kJ��mol-1��H��H���ļ�����436��0kJ��mol-1����N2��H2�ϳ�1molNH3ʱ�ɷų�46��2kJ����������N��H���ļ�����_____________��
�ο��𰸣���1��N2H4(l)+2H2O2(l)==N2(g)+4H2O(g) ��H��-641.75KJ/mol��408.875KJ�����ﲻ����ɻ�����Ⱦ
��2��391.6 kJ��mol-1
���������
�����Ѷȣ�һ��
2������� ����ú��ƶ�͡����������ҹ���Դ��չ���ٵ���״��������Դ��������ţ���չ��ú���������ҹ���Դ�ṹ�ĵ���������Ҫ���塣��ͼ��ú������ҵ��֮һ��
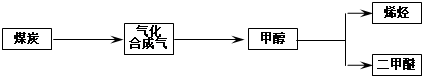
���ྻú�������о����������൱�ձ飬������Աͨ�������ú������¯�н�����������ˮ�����ķ���������������ֵ�ܸߵ�ú̿�ϳ���������Ҫ�ɷ���CO��H2��CO��H2����Ϊ��Դ�ͻ���ԭ�ϣ�Ӧ��ʮ�ֹ㷺��
��1����֪��C(s)+O2(g)=CO2(g) ��H1����393.5 kJ��mol
�ο��𰸣�
���������
�����Ѷȣ�����
3��ѡ���� �����Ȼ�ѧ����ʽ��д��ȷ���ǣ� ? ��
A��2SO2+O2?2SO3����H=-196.6kJ/mol
B��C��s��+O2��g���TCO2��g������H=393.5kJ/mol
C��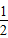 H2��g��+
H2��g��+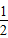 Cl2��g���THCl��g������H=-92.5kJ/mol
Cl2��g���THCl��g������H=-92.5kJ/mol
D��H+��aq��+OH-��aq���TH2O��l������H=57.3kJ
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4������� ��14�֣���ҵ���Դ�ʳ�Σ���������Ca2+��Mg2+���ʣ�������ʯ��ʯ��Ϊԭ�ϣ������Ʊ�Na2CO3�����������ͼ��ʾ��
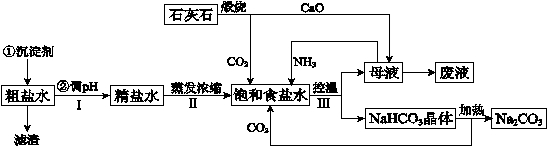
��ش�
��1���ڴ�������ˮ�Ĺ����У��ɼ���ʯ����ʹ�����Ϊ�������������������ijɷֳ������ij�������� ��
��2����CaOͶ�뺬�д�����NH4Cl��ĸҺ�У������ɿ�ѭ��ʹ�õ�NH3���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3����ʳ��ˮ������ͨ��������� �����̢�������NaHCO3����ķ�Ӧ�Ļ�ѧ����ʽ�� ��
��4��̼���ƾ���ʧˮ�������仯ʾ��ͼ���£�

Na2CO3��H2O (s) ��ˮ��Ӧ���Ȼ�ѧ����ʽ�� ��
��5����Ʒ�����г�����NaCl��ȡa g�����������ϡ�����ַ�Ӧ�����ȡ����ɡ����գ���b g���塣��ò�Ʒ��Na2CO3������������ ��
��6������Na2CO3�������顪������ȼ�ϵ�صĵ���ʣ��õ�ظ����ķ�Ӧʽ�� ��
�ο��𰸣�(14�֣�ÿ��2��)
��1��CaCO3��Mg(OH)2��©д��1�֣������0�֣�
��2��2NH4Cl+CaO=CaCl2+2NH3��+2H2O
��3��NH3 �� NH3+H2O+CO2+NaCl =NaHCO3��+NH4Cl
��4��Na2CO3��H2O(s)= Na2CO3(s) +H2O(g) ��H=" +" 58.73 kJ��mol��1
��5��106(b��a)/11a
��6��CH4��8e��+4CO32��=5CO2+2H2O
�����������1�������еĸơ�þ���ӿ���ʯ����ʹ��Ӧ����̼��ƺ�������þ���������������ijɷֳ������ij��������CaCO3��Mg(OH)2��
��2��CaOͶ��ˮ�������������ƣ����Ȼ�立�Ӧ�����������Ȼ��ơ�ˮ�����Ը÷�Ӧ�Ļ�ѧ����ʽ��2NH4Cl+CaO=CaCl2+2NH3��+2H2O��
��3����Ϊ������̼��ˮ�е��ܽ�Ȳ���������ͨ�백����������Һ�ļ��ԣ���ͨ�������̼���壻������������̼�뱥��ʳ��ˮ��Ӧ�����Ȼ�狀�̼�����Ƴ�������ѧ����ʽ��NH3+H2O+CO2+NaCl =NaHCO3��+NH4Cl��
��4������̼���ƾ���ʧˮ�������仯ʾ��ͼ��֪��Na2CO3��10H2O(s)= Na2CO3(s) +10H2O(g) ��H=+532.36kJ/mol��Na2CO3��10H2O(s)= Na2CO3��H2O (s) +9H2O(g) ��H=+473.63kJ/mol�����ݸ�˹���ɣ���ʽ���Na2CO3��H2O (s) ��ˮ��Ӧ���Ȼ�ѧ����ʽ��Na2CO3��H2O(s)= Na2CO3(s) +H2O(g) ��H=+532.36kJ/mol-��+473.63kJ/mol��="+" 58.73 kJ��mol��1��
��5��̼���������ᷴӦ���������ơ�ˮ�Ͷ�����̼���������ɺ�õ��Ĺ���Ϊ�Ȼ��ƣ�������Ӧ�Ļ�ѧ����ʽ�ǣ�Na2CO3+2HCl=2NaCl+CO2��+H2O�����ò�����������Ʒ��̼���Ƶ�������x����
Na2CO3+2HCl=2NaCl+ CO2��+ H2O ����������
106 117 117-106=11
x (b-a)g
����106:11=x����b-a��g�����x=106��b-a��/11g����ò�Ʒ��Na2CO3������������106��b-a��/11g/ag=106(b��a)/11a��
��6��������̼����������ʣ�����ȼ�ϵ���У���������������Ӧ��������ڸ�������������Ӧ��ʧȥ���ӣ����ɶ�����̼��ˮ�����Ը����ĵ缫��Ӧʽ��CH4��8e��+4CO32��=5CO2+2H2O��
���㣺���������Ƽ�Ĺ������̣���˹���ɵ�Ӧ�ã��绯ѧ��Ӧԭ����Ӧ��
�����Ѷȣ�����
5������� ��10�֣��Իش����и����⣺
��1����ͼ����ʾ��1 mol NO2��CO��Ӧ���� CO2��NO�����������仯ʾ��ͼ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ�� ��
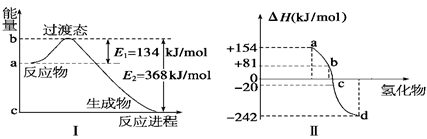
��2����ѧ��Ӧ���ʱ��뷴Ӧ���������ļ����йء�
����֪��H2(g)+Cl2(g) ="==" 2HCl(g) ��H="-185" kJ/mol;
���ܦ�H298(H��H)="436" kJ/mol,��H298(Cl��Cl)="247" kJ/mol,��H298(H��Cl)= ��
��ͼ���ʾ����Ԫ���е���������(Se)���������⻯��ʱ���ʱ����ݣ����������ʱ����ݿ�ȷ��a��b��c��d�ֱ������Ԫ�أ���д�������ⷢ���ֽⷴӦ���Ȼ�ѧ����ʽ�� ��
��3����֪�� ��Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g) ��H="-a" kJ/mol
2Fe(s)+3CO2(g) ��H="-a" kJ/mol
��3Fe2O3(s)+CO(g)  2Fe3O4(s)+CO2(g) ��H="-b" kJ/mol
2Fe3O4(s)+CO2(g) ��H="-b" kJ/mol
��Fe3O4(s)+CO(g)  3FeO(s)+CO2(g) ��H="+ckJ/mol"
3FeO(s)+CO2(g) ��H="+ckJ/mol"
��FeO(s) +CO(g)  Fe(s)+CO2(g) ��H=- ��
Fe(s)+CO2(g) ��H=- ��
�ο��𰸣���1��NO2(g)+CO(g) ="==" NO(g)+CO2(g) ��H="-234" kJ/mol
��2����434 kJ/mol����H2Se(g) ="==" Se(s)+H2(g) ��H="-81" kJ/mol
��3����H= ��1/6��3a��b��2c��kJ/mol
�����������1������ͼ���֪��Ӧ�����������������������������Ƿ��ȷ�Ӧ���ų���������368kJ/��134 kJ��234 kJ�������Ȼ�ѧ����ʽΪNO2(g)+CO(g) ="==" NO(g)+CO2(g) ��H="-234" kJ/mol��
��2���ڷ�Ӧ�Ⱦ��Ƕϼ����յ��������γɻ�ѧ�����ų��������IJ�ֵ����˦�H="=436" kJ/mol��247 kJ/mo��2X����185 kJ/mo�����X��434 kJ/mol��
�ٷǽ�����Խǿ������������Խ���ң��ų���������Խ�ࡣ����a��b��c��d�ֱ������Ԫ�����ڡ���(Se) ������������������ķ�Ӧ�����ȷ�Ӧ�����淴Ӧ���Ƿ��ȷ�Ӧ�����������ⷢ���ֽⷴӦ���Ȼ�ѧ����H2Se(g) ="==" Se(s)+H2(g) ��H="-81" kJ/mol��
��3�����ݸ�˹���ɿ�֪���١�3���ڣ��ۡ�2���õ�6FeO(s) +6CO(g)  6Fe(s)+6CO2(g)�����Է�Ӧ��Ϊ��H= ����3a��b��2c��kJ/mol��
6Fe(s)+6CO2(g)�����Է�Ӧ��Ϊ��H= ����3a��b��2c��kJ/mol��
�����Ѷȣ�һ��