|
�߿���ѧ֪ʶ���ܽᡶ�й�������ԭ��Ӧ�ļ��㡷���߲��ԣ�2019�����°棩(ʮ)
2019-06-25 23:16:09
�� �� �� ��
|
1��ѡ���� ���ڷ�ӦKClO3+ HCl �� KC1 + Cl2 ��+ H2O��δ��ƽ������0��1 mol KClO3�μӷ�Ӧ������˵����ȷ���� ( )
A��ת��0��5 mol����
B������0��1 mol Cl2
C����������HC1Ϊ0��6 mol
D��Cl2��ֻ���������ﲻ�ǻ�ԭ����
|
�ο��𰸣�A
����������÷�Ӧ�����������Ԫ�ػ��ϼ���+5�۱�Ϊ0�ۣ���������Ԫ�صĻ��ϼ���-1�۱�Ϊ0�ۣ�����ת�Ƶ�����ȡ�ԭ���غ���ƽ����ʽ��KClO3+ 6HCl �� KC1 + 3Cl2 ��+ 3H2O��A������0.1mol0��1 mol KClO3�μӷ�Ӧ��ת�Ƶ��ӵ����ʵ���0.5mol����ȷ��B������0.1mol0��1 mol KClO3�μӷ�Ӧ������0��3 mol Cl2������C������0.1mol0��1 mol KClO3�μӷ�Ӧ�����������Ȼ�������ʵ���0.5mol������D��Cl2�Ǽ��������������ǻ�ԭ�������
���㣺����������ԭ��Ӧ��
�����Ѷȣ�һ��
2������� ������и��⣮
��1��NaHCO3���������ij������ɼ���д��NaHCO3���ȷֽ�Ļ�ѧ����ʽ______��
��2��CH4��Cl2�ڹ���������������CH3Cl��д���÷�Ӧ�Ļ�ѧ����ʽ______��
�ο��𰸣���1��̼���������ȷֽ��̼���ơ�ˮ�Ͷ�����̼���÷�ӦΪ2NaHCO3?����?.?Na2CO3+CO2��+H2O����
�ʴ�Ϊ��2NaHCO3?����?.?Na2CO3+CO2��+H2O��
��2��CH4��Cl2�ڹ���������������CH3Cl��HCl���÷�ӦΪCH4+Cl2��
���������
�����Ѷȣ�һ��
3��ѡ���� ��ͬ�¶Ⱥ�ѹǿ�£�3�����X2������6�����Y2���廯������6�������̬������A����������A�Ļ�ѧʽΪ?(? )
A��XY2
B��X3Y2
C��X2Y3
D��XY
�ο��𰸣�A
�����������������ͬ�¶Ⱥ�ѹǿ�£���ͬ������κ����庬����ͬ��Ŀ�ķ��ӡ���ϻ�ѧ��Ӧ�Ĺ��̾���ԭ��������ϵĹ��̡��ɵã�3X2+6Y2=6XY2������̬������A�Ļ�ѧʽΪ��XY2��ѡ��ΪA��
�����Ѷȣ�һ��
4������� H2O2�ڹ�ҵ��ũҵ��ҽҩ�϶��й㷺����;��
��1��H2O2�Ƕ�Ԫ���ᣬд����һ���ĵ��뷽��ʽ?���ڶ����ĵ���ƽ�ⳣ������ʽKa2��?��
��2���������ʶ�������H2O2�ֽ�Ĵ�����һ�ֹ۵���Ϊ���ڷ�Ӧ�����д����ȱ�H2O2��������ԭ�������ֱ�H2O2��ԭ�������������������ʶ�����H2O2�ֽ�Ĵ������ڷ�Ӧ�������ȱ���������ԭ����?��
��I��?��Fe3��?��Cu2��?��Fe2��
��3���ü�������ȼ�ϵ�غϳ�H2O2������Ч�ʸߣ�����Ⱦ���ص㡣����ܷ�ӦΪ��
H2 + O2 + OH�� �� H2O + HO2����д��������Ӧʽ��?��
��4��H2O2��һ�ֻ����Ѻõ�ǿ����������Ʒ�ˮ����Ҫ��Cu2����Ni2������������Fe3����Fe2����Cr3�� �ȣ��Ʊ���������һ���������£�
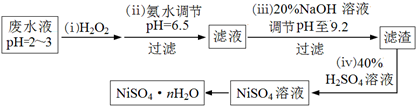
�ٵڣ�������������H2O2��Ӧ�����ӷ���ʽ?��
�ڵڣ��������������е���Ҫ�ɷ���ҽ���ϵ���;��?��
��Ϊ�ⶨNiSO4��n H2O����ɣ���������ʵ�飺��ȡ2.627g��Ʒ�����Ƴ�250.00 mL��Һ��ȷ��ȡ���Ƶ���Һ25.00 mL����0.04000 mol��L��1��EDTA��Na2H2Y������Һ�ζ�Ni2+�����ӷ���ʽΪNi2��+ H2Y2����NiY2��+ 2H����������EDTA����Һ25.00 mL��������������Ļ�ѧʽΪ?��
�ο��𰸣���1��H2O2 H�� + HO2����2�֣�? H�� + HO2����2�֣�?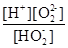 �� ��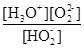 ��3�֣� ��3�֣�
��2���٢ܣ�2�֣�
��3��O2 + H2O + 2e�� �� HO2��+ OH�� ��3�֣�
��4����2H��+ 2Fe2��+ H2O2 �� 2Fe3��+ 2H2O��3�֣�
�����ǵļ�⣨2�֣�
��NiSO4��6H2O ��3�֣�
�����������1����һ�����룬1��H2O2�����1��H+�����뷽��ʽΪ��H2O2 H�� + HO2�����ڶ�������Ϊ��HO2- H�� + HO2�����ڶ�������Ϊ��HO2-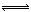 O22?+H+�����Ե���ƽ�ⳣ��Ka2�� O22?+H+�����Ե���ƽ�ⳣ��Ka2��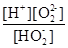 �� ��
��2���ڷ�Ӧ�������ȱ���������ԭ��˵�������ʾ��л�ԭ�ԣ�I?��Fe2+���н�ǿ�Ļ�ԭ�ԣ��ʢ٢���ȷ��
��3������ΪO2�õ��ӣ������ܷ�Ӧ����ʽ��O2��OԪ�ػ��ϼ۽���ת��ΪHO2������������Ӧ����ʽΪ��O2 + H2O + 2e�� �� HO2��+ OH��
��4���ٷ�ˮ�к���Fe2+�����л�ԭ�ԣ���H2O2���������ӷ���ʽΪ��2H��+ 2Fe2��+ H2O2 �� 2Fe3��+ 2H2O
�ڵڣ��������������е���Ҫ�ɷ�ΪCu(OH)2����ҽ���Ͽ��������ǵļ�⡣
�۸��ݷ���ʽ��Ni2��+ H2Y2����NiY2��+ 2H����ԭ��Ʒ��NiSO4�����ʵ���Ϊ��0.04000mol/L��0.025L��250/25=0.01mol��������ʵ�Ħ������Ϊ��2.627g��0.01mol=262.7g/mol,�ᾧˮ��ϵ��Ϊ����262.7-154.7����18=6�����Ի�ѧʽΪ��NiSO4��6H2O
�����Ѷȣ�һ��
5��ѡ���� �����йػ�ѧ�����ʾ��ȷ���ǣ���������
A����������ķ���ʽ��SiO2
B������ϩ�Ľṹ��ʽ��?CH2CH2?
C���������ƣ�NaClO4����ClԪ�صĻ��ϼۣ���6
D��Mg5��Si4O10��2��OH��2��4H2O����������ʽ��5MgO��8SiO2��5H2O
�ο��𰸣�BD
���������SiO2��ԭ�Ӿ��壬��SiO2���ӣ�A����C�����������Na�ԣ�1�ۣ�O�ԣ�2�ۣ���Cl�ԣ�7�ۣ�����
�����Ѷȣ�һ��
|