1、选择题 鉴别纯碱、石灰石、芒硝、石膏四种固体物质,下列试剂中应该选用(?)
A.NaOH溶液
B.水、盐酸
C.硝酸溶液
D.BaCl2和HNO3的混合液
参考答案:B
本题解析:芒硝为Na2SO4・10H2O,石膏为CaSO4・2H2O,后者不溶于水,故加水分成两组,再加盐酸检验。
本题难度:简单
2、选择题 下列反应中,SO2不是作为还原剂而发生反应的是
?
A.2SO2+O22SO3
B.SO2+H2O H2SO3
H2SO3
C.SO2+2H2S====3S↓+2H2O
D.SO2+Cl2+2H2O====H2SO4+2HCl
参考答案:BC
本题解析:A项中SO2被氧化作还原剂,B项为非氧化还原反应,C项中SO2被还原作氧化剂,D项中SO2被氧化作还原剂。
本题难度:简单
3、选择题 某同学利用下列装置进行浓硫酸和铜反应并验证二氧化硫的性质。按如图实验装置连接仪器和放置药品。加热浓硫酸约1分钟后撤去酒精灯,将铜丝插入液面,反应一段时间后拔出。实验结束后会看到两个试管的液体底部均有少量的白色固体。下列对该实验的现象分析或推断正确的是

A.湿润的蓝色石蕊试纸先变红后褪色
B.左边试管出现的白色固体是由于浓硫酸的脱水性所致
C.从该实验的描述中可以体会出铜与浓硫酸的反应是一个放热反应
D.本实验体现了二氧化硫的酸性、漂白性和弱氧化性
参考答案:C
本题解析:A、SO2不能漂泊石蕊,所以蓝色石蕊试纸变红,不会褪色,错误;B、Cu与浓硫酸反应生成CuSO4,左边试管出现的白色固体为无水CuSO4,错误;C、加热浓硫酸约1分钟后撤去酒精灯,反应继续进行,说明铜与浓硫酸的反应是放热反应,正确;D、湿润的蓝色石蕊试纸变红,体现了SO2溶于水后显酸性,吸有品红溶液的滤纸褪色,体现了SO2的漂白性,但本实验无法证明二氧化硫的弱氧化性,错误。2的性质。
本题难度:一般
4、选择题 向下列溶液中通入足量SO2的过程中,一定不会产生沉淀的是?(?)
A.Ba(OH)2
B.Ba( NO3)2
C.Na2S
D.BaCl2
参考答案:D
本题解析:略
本题难度:一般
5、选择题 在标准状况下,向100 mL氢硫酸溶液中通入二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为( )?
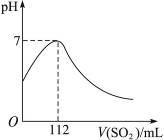
A.0.5 mol・L-1?
B.0.05 mol・L-1?
C.1 mol・L-1?
D.0.1 mol・L-1?
参考答案:D
本题解析:氢硫酸和二氧化硫反应如下:2H2S+SO2====3S+2H2O。开始时,氢硫酸显酸性,pH小于7;加入二氧化硫时,反应生成中性物质,pH逐渐升高;恰好完全反应时,呈中性,pH等于7。由方程式可得c(H2S)="2×0.005" mol÷0.1 L="0.1" mol・L-1。
本题难度:简单