1、填空题 A、B代表不同的物质,都是H、N、O、Na中的任意三种元素组成的强电解质,A的水溶液呈碱性,B的水溶液呈酸性,请找出A、B可能的两种组合。要求:相同浓度时,A1溶液中水的电离程度小于A2溶液中水的电离程度;相同浓度时,B1溶液中水的电离程度小于B2溶液中水的电离程度。请填写下列空白:
(1)写出化学式:A1___________、A2__________、B1___________、B2___________。
(2)相同温度下,当A1、B1的物质的量浓度相等时,两种溶液中水电离出的氢离子的物质的量浓度之比为________。
(3)0.1mol?L-1NaNO2溶液中离子浓度由大到小的顺序为___________________________________。
(4)B1溶液中水的电离程度小于B2溶液中水的电离程度,原因是___________。
(5)常温下,若B1、B2两种溶液的pH=5,则两溶液中由水电离出的氢离子的物质的量浓度之比为________。
参考答案:(1)NaOH;NaNO2;HNO3;NH4NO3(2)1∶1(3)c(Na+)>c(NO2-) >c(OH-)>c(H+)
(4)硝酸电离出的氢离子抑制了水的电离,NH4+的存在促进了水的电离 (5)1×10-4∶1
本题解析:(1)根据给出的元素:H、N、O、Na,其中由三种元素组成的强电解质,中学化学常见物质有:强碱(NaOH)、强酸(HNO3);盐:NaNO3、NaNO2、NH4NO3、NH4NO2等。A显碱性,只可能是NaOH和NaNO2,B显酸性,可能是HNO3和NH4NO3。强酸、强碱都抑制水的电离,而易水解的盐则促进水的电离。相同浓度时,A1溶液中水的电离程度小于A2溶液中水的电离程度,故A1为NaOH,A2为NaNO2;相同浓度时,B1溶液中水的电离程度小于B2溶液中水的电离程度,故B1为HNO3,B2为NH4NO3。
(2)强酸或强碱溶液中氢离子或OH-浓度在相等的条件下对水电离的抑制程度是相同,则两种溶液中水电离出的氢离子的物质的量浓度之比为1∶1。
(3)亚硝酸钠是强碱弱酸盐,水解溶液显碱性,则溶液中离子浓度由大到小的顺序为c(Na+)>c(NO2-) >c(OH-)>c(H+)。
(4)由于硝酸电离出的氢离子抑制了水的电离,而NH4+的水解促进了水的电离,所以B1溶液中水的电离程度小于B2溶液中水的电离程度。
(5)硝酸抑制水的电离,硝酸铵促进水的电离,所以如果两种溶液的pH=5,则两溶液中由水电离出的氢离子的物质的量浓度之比为10-9:10-5=1×10-4∶1。
点评:该题是高考中的常见考点和题型,属于中等难度试题的考查,试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生解题能力的培养,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。该题解题的关键是明确外界条件对水的电离平衡的影响,然后结合题意灵活运用即可。
本题难度:一般
2、选择题 下列各变化的方程式中,属于水解反应的是:
A. H2O +H2O H3O+ +OH-
H3O+ +OH-
B.HCO3- +OH- H2O +CO32-
H2O +CO32-
C. CO2 +H2O H2CO3
H2CO3
D.CO32- +H2O
 HCO3- +OH-
HCO3- +OH-
参考答案:D
本题解析:略
本题难度:一般
3、填空题 (8分)向Na2CO3溶液中滴加酚酞呈红色的原因是? ?(用离子方程式表示);溶液中各离子浓度由大到小的顺序?;向此溶液中加入AlCl3溶液,观察到的现象是?,反应的离子方程式为?。
?(用离子方程式表示);溶液中各离子浓度由大到小的顺序?;向此溶液中加入AlCl3溶液,观察到的现象是?,反应的离子方程式为?。
参考答案:CO32-+H2O ? HCO3-+OH-;c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+);
? HCO3-+OH-;c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+);
有气泡及白色沉淀 产生,溶液红色逐渐变浅至颜色消失;
产生,溶液红色逐渐变浅至颜色消失;
2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑
本题解析:略
本题难度:一般
4、填空题 在配制Al2(SO4)3溶液时,铝离子会部分水解而使溶液呈酸性,水解的离子方程式为:?。为了防止发生水解,可以加入少量的?;在Na2S溶液中,硫离子水解的离子方程是 ??;为了防止水解,在配制该溶液时,可以加入少量的 ??。
参考答案:Al3+ +3H2O 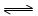 Al(OH)3+3H+?稀硫酸
Al(OH)3+3H+?稀硫酸
 ?S2- + H2O?
?S2- + H2O?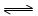 HS- + OH-?氢氧化钠
HS- + OH-?氢氧化钠
本题解析:略
本题难度:简单
5、选择题 已知某温度下0.1mol/L的NaHB(强电解质)溶液中c(H+)>c(OH-),则下列关系一定正确的是(? )
A.c(Na+)=c(HB-)+2c(B2-)+c(OH-)
B.c(Na+)=0.1mol/L≥c(B2-)
C.c(H+)・c(OH-)=10-14
D.溶液的PH等于1
参考答案:B
本题解析:由NaHB是强电解质和c(H+)>c(OH-),但并不知道HB-是完全电离还是部分电离,只知可能完全电离或部分电离时应电离程度大于水解程度,故B正确,而D错误;依据电荷守恒知A错;又C项中某温度并非是常温。
本题难度:一般