1、选择题
|
下图各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是
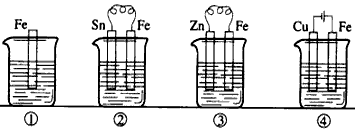
[? ]
A.④>②>①>③
B.④>②>③>①
C.②>①>③>④
D.③>②>④>①
参考答案:A
本题解析:
本题难度:一般
2、选择题 下列说法正确的是
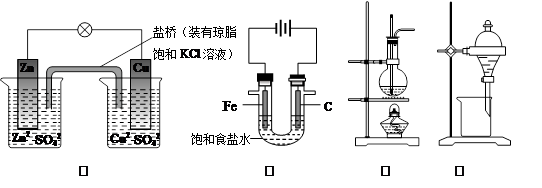
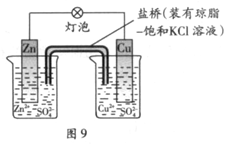
A.图①铜锌原电池工作时,盐桥中的K+移向ZnSO4溶液
B.图②装置反应一段时间,将湿润的KI淀粉试纸靠近碳电极管口,试纸变蓝
C.图③是用海水制取蒸馏水的装置
D.图④装置可用于乙醇提取碘水中的碘
参考答案:B
本题解析: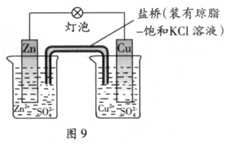 A.图盐桥中的K+移向正极方向移动,应该是向CuSO4溶液方向移动,错误;;C.图③是用海水制取蒸馏水不要用到温度计,错误;D.乙醇与水相互溶解不能分层,所以无法提取碘水中的碘,错误;
A.图盐桥中的K+移向正极方向移动,应该是向CuSO4溶液方向移动,错误;;C.图③是用海水制取蒸馏水不要用到温度计,错误;D.乙醇与水相互溶解不能分层,所以无法提取碘水中的碘,错误;
本题难度:一般
3、选择题 下图装置中,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片。观察:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面。以下有关解释合理(?)

A.生铁片中的碳是原电池的阳极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.墨水回升时,碳极反应式为:O2 + 2H2O + 4e―= 4OH―
D.具支试管中溶液pH逐渐减小
参考答案:C
本题解析:酸性较强时,铁片可直接置换出氢离子,同时可发生析氢腐蚀,内部压强增大,导管内液面下降;当酸性较弱甚至接近于中性时,发生吸氧腐蚀,O2 + 2H2O + 4e―= 4OH―,内部压强减小,导管内液面上升。
本题难度:一般
4、填空题 电解是最强有力的氧化还原手段,在化工生产中有着重要的应用。请回答下列问题:
(1)以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为________,阴极反应式为________。
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是
_______(填序号)。

a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2OCH3CH2OH+CH3COOH
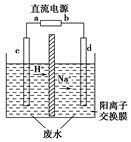
实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入________(填化学式),电极反应式为________。电解过程中,阴极区Na2SO4的物质的量________(填“增大”、“减小”或“不变”)。
②在实际工艺处理中,阴极区乙醛的去除率可达60%。若在两极区分别注入1 m3乙醛含量为3 000 mg/L的废水,可得到乙醇________kg(计算结果保留小数点后一位)。
参考答案:(1)2Cu+H2O-2e-=Cu2O+2H+ 2H++2e-=H2↑ (2)d (3)①CH4 CH4-8e-+10OH-=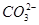 +7H2O 不变 ②1.9
+7H2O 不变 ②1.9
本题解析:(1)由于阳极材料为铜,所以铜本身失电子被氧化,由题意知氧化产物为Cu2O,可得阳极反应式为2Cu+H2O-2e-=Cu2O+2H+,阴极上阳离子放电,即溶液中H+被还原成清洁能源H2。
(2)左半区是原电池装置,发生的是铁的吸氧腐蚀,负极(Fe):Fe-2e-=Fe2+,正极(Cu):O2+2H2O+4e-=4OH-。右半区是电解装置,阳极(Fe):Fe-2e-=Fe2+,阴极(Cu):2H++2e-=H2↑,由于电解引起腐蚀的速率远大于吸氧腐蚀的速率,因此最先观察到变成红色的区域是④区,故选项a、b、c均错误。
(3)①根据电解液中阳离子的迁移方向,可知c为阳极,d为阴极,因此直流电源上a为正极,通入O2,b为负极,通入CH4,在碱性条件下CH4的氧化产物为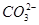 ,由此可写出此电极的电极反应式。在电解过程中,由于
,由此可写出此电极的电极反应式。在电解过程中,由于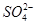 没有参与放电,且阳离子交换膜不允许阴离子自由通过,因此根据质量守恒可得阴极区Na2SO4的物质的量不变。
没有参与放电,且阳离子交换膜不允许阴离子自由通过,因此根据质量守恒可得阴极区Na2SO4的物质的量不变。
②阴极区发生还原反应,即CH3CHO转化成CH3CH2OH,设生成的乙醇为x kg,根据碳原子守恒可得关系式:
CH3CHO ~ CH3CH2OH
44? ? 46
3 000×103÷106×60%? x
解得x≈1.9。
本题难度:一般
5、选择题 下列叙述不正确的是(?)
A.电解法精炼铜时粗铜连接电源的正极
B.船底镶嵌锌块,锌作负极,以防船体被腐蚀
C.铜锌原电池中铜电极上发生氧化反应
D.工业上电解饱和食盐水的阳极反应:2Cl- ―2e -=Cl2↑
参考答案:C
本题解析:A.电解法精炼铜时粗铜连接电源的正极作阳极,精铜连接电源的负极作阴极。正确。B.由于锌的金属性比铁强,当在船底镶嵌锌块时,首先是活动性比铁强的锌失去电子,作负极,对船体来说就起到了保护作用,可以防船体被腐蚀。正确。C.铜锌原电池中铜电极上发生还原反应,锌电极上发生氧化反应。错误。D.工业上电解饱和食盐水的阳极反应:2Cl- ―2e -=Cl2↑,阴极反应2H2O+2e-=2OH-+H2↑.正确。
本题难度:一般