1、选择题 血红蛋白的相对分子质量约为68000,已知其中含铁的质量分数为0.33%,则平均每个血红蛋白的分子中铁原子数约为?(?)
A.5
B.4
C.3
D.2.408×1024
2、选择题 将5.6g铁溶于足量稀盐酸中,再加入足量的氢氧化钠溶液,充分反应,过滤;在空气中加热所得滤渣,灼烧到质量不再变化,此时固体的质量为
A.7.2g
B.8.0g
C.9.0g
D.10.7g
3、选择题 在热的稀硫酸溶液中溶解了11.4g FeSO4,当加入50mL 0.5mol・L-1KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3溶液也完全反应,并有NxOy气体逸出,则该NxOy是?
A.N2O
B.NO
C.N2O3
D.NO2
4、选择题 要除去FeCl2溶液中的少量氯化铁,可行的办法是(? )
A.滴入KSCN溶液
B.加入铁粉
C.加入铜粉
D.通入氯气
5、简答题 三氯化铁是中学化学实验室中常用的化学试剂.某同学利用废铁屑(含少量铜等不与盐酸反应的杂质)来制备FeCl3?6H2O,该同学设计的实验装置如图所示,其实验步骤如下:A中放有废铁屑,烧杯中盛有过量的稀硝酸,实验时打开a,关闭b,从分液漏斗内向A中加过量的盐酸,此时溶液呈浅绿色,再打开b进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分水并使剩余HNO3分解,再降温结晶得FeCl3?6H2O晶体.填写下列空白:
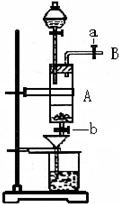
(1)收集导管B处的气体可采用的方法是______.滴加盐酸时,发现反应速率较之盐酸与纯铁粉反应要快,其原因是______.
(2)烧杯内放过量稀HNO3的原因是______.发生反应的离子方程式是______.
(3)整个实验过程中,弹簧夹a都必须打开,除为排出产生的气体外,另一个目的是______.
(4)将烧杯内溶液用蒸发、浓缩、再降温结晶法制得FeCl3?6H2O,而不用直接蒸干的方法来制得晶体的理由是______
(5)你认为该实验存在的缺点可能有:______.