1��ѡ���� Ѫ�쵰����Է�������ԼΪ68000����֪���к�������������Ϊ0.33%����ƽ��ÿ��Ѫ�쵰�ķ�������ԭ����ԼΪ?��?��
A��5
B��4
C��3
D��2.408��1024
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
2��ѡ���� ��5.6g����������ϡ�����У��ټ�������������������Һ����ַ�Ӧ�����ˣ��ڿ����м����������������յ��������ٱ仯����ʱ���������Ϊ
A��7.2g
B��8.0g
C��9.0g
D��10.7g
�ο��𰸣�B
���������5.6g�������ʵ�����5.6g��556g/mol��0.1mol���������ᷴӦ�����Ȼ���������������������������������Һ������������������ɫ�������������������ȶ������ձ�ת��Ϊ���������������������ȷֽ�������������ˮ�����Ը�����ԭ���غ��֪�����������ʵ�����0.1mol��2��0.05mol��������0.05mol��160g/mol��8.0g����ѡB��
�����Ѷȣ�һ��
3��ѡ���� ���ȵ�ϡ������Һ���ܽ���11.4g FeSO4��������50mL 0.5mol��L��1KNO3��Һ��ʹ���е�Fe2+ȫ��ת����Fe3+��KNO3��ҺҲ��ȫ��Ӧ������NxOy�����ݳ������NxOy��?
A��N2O
B��NO
C��N2O3
D��NO2
�ο��𰸣�B
���������11.4g FeSO4�����ʵ���Ϊ0.075mol������Ӧ��ȫ��ת�Ƶĵ��ӵ����ʵ���Ϊ0.075mol��50mL 0.5mol��L��1KNO3�����ʵ���Ϊ0.025 mol���跴Ӧ��NԪ�صĻ��ϼ�Ϊx������ ����
����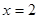 ��������ȷѡ��ΪB��
��������ȷѡ��ΪB��
�����Ѷȣ�һ��
4��ѡ���� Ҫ��ȥFeCl2��Һ�е������Ȼ��������еİ취��(? )
A������KSCN��Һ
B����������
C������ͭ��
D��ͨ������
�ο��𰸣�B
���������A��KSCN��Һ�Ǽ������������ӵ��Լ������ܳ��ӣ����������ۣ����ۺ��Ȼ�������FeCl2�����У�C��ͭ�ۺ��Ȼ�������FeCl2��CuCl2�������µ����ʣ�����D���������FeCl2����ΪFeCl3�������С�
������ע�������и����ʵ����ʣ�����ת����Ӧ���ӣ�ע�ⲻ�������µ����ʣ�Ҳ���ܰ���Ҫ���ʷ�Ӧ��
�����Ѷȣ�һ��
5������� ���Ȼ�������ѧ��ѧʵ�����г��õĻ�ѧ�Լ���ijͬѧ���÷���м��������ͭ�Ȳ������ᷴӦ�����ʣ����Ʊ�FeCl3?6H2O����ͬѧ��Ƶ�ʵ��װ����ͼ��ʾ����ʵ�鲽�����£�A�з��з���м���ձ���ʢ�й�����ϡ���ᣬʵ��ʱ��a���ر�b���ӷ�Һ©������A�мӹ��������ᣬ��ʱ��Һ��dz��ɫ���ٴ�b���й��ˣ����˽�����ȡ�ձ�����Һ������������ȣ�����������ˮ��ʹʣ��HNO3�ֽ⣬�ٽ��½ᾧ��FeCl3?6H2O���壮��д���пհף�
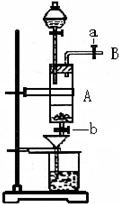
��1���ռ�����B��������ɲ��õķ�����______���μ�����ʱ�����ַ�Ӧ���ʽ�֮�����봿���۷�ӦҪ�죬��ԭ����______��
��2���ձ��ڷŹ���ϡHNO3��ԭ����______��������Ӧ�����ӷ���ʽ��______��
��3������ʵ������У����ɼ�a���������Ϊ�ų������������⣬��һ��Ŀ����______��
��4�����ձ�����Һ��������Ũ�����ٽ��½ᾧ���Ƶ�FeCl3?6H2O��������ֱ�����ɵķ������Ƶþ����������______
��5������Ϊ��ʵ����ڵ�ȱ������У�______��
�ο��𰸣���1������B��������Ϊ�����������ܶȱȿ���С�Ҳ�����ˮ��������ˮ���������ſ������ռ���Cu�����γ�Fe-Cuԭ���ʹ��Ӧ���ʼӿ죬
�ʴ�Ϊ������ˮ���������ſ������������м�к�����Cu�����ʣ��γ�Fe-Cuԭ���ʹ��Ӧ���ʼӿ죻
��2��������ϡHNO3��֤ʹFe2+ ȫ��������Fe3+����Ӧ�����ӷ���ʽ��3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��
�ʴ�Ϊ��ϡHNO3��ǿ�����ԣ�Ϊ��֤ʹFe2+ȫ��������Fe3+��3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��
��3��ʹ��Һ©���е���ɵ���A�У��ʴ�Ϊ���������ͨ��ʹ��Һ©���е���ɵ���A�У�
��4����ΪFeCl3��ǿ��������ˮ�⣬��������ʱʹHCl�ӷ����ˮ��ƽ�����ƣ���˵ò���FeCl3?6H2O��
�ʴ�Ϊ����ΪFeCl3��ǿ��������ˮFeCl3+3H2O?Fe��OH��3+3HCl����������ʱʹHCl�ӷ����ˮ��ƽ�����ƣ���˵ò���FeCl3?6H2O��
��5����β������װ�ã���ϡHNO3����FeCl2ʱ���������������ʹ�Ƶõ�FeCl3?6H2O������
�ʴ�Ϊ����Ӧ�в������к��������Ⱦ��������ϡHNO3����FeCl2ʱ����Fe��NO3��3���ɶ�ʹ�Ƶõ�FeCl3?6H2O������
���������
�����Ѷȣ�һ��