1、填空题 (10分) 25℃时,电离平衡常数:
化学式
| CH3COOH
| H2CO3
| HClO
| H2C4H4O6(酒石酸)
| H2SO3
|
电离平衡常数
| 2.0×10-5
| K1=4.3×10-7
K2=5.6×10-11
| 3.0×10-8
| K1=9.1×10-4
K2=4.3×10-5
| K1=1.3×10-2
K2=6.3×10-8
|
回答下列问题:
(1)pH相同的下列物质的溶液:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3,e.Na2C4H4O6;物质的量浓度由大到小的顺序是 (填字母)。
(2)常温下,0.1mol/L的CH3COOH溶液的pH== (已知lg2=0.3)。
(3)常温下,将0.1mol/L的次氯酸溶液与0.1mol/L的碳酸钠溶液等体积混合,所得溶液中各种离子浓度关系正确的是
A.c(Na+) > c(ClO-) >c(HCO3-) >c(OH-)
B.c(Na+) > c(HCO3-)>c(ClO-) > c(H+)
C.c(Na+) ==" c(HClO)" +c(ClO-)+ c(HCO3-) + c(H2CO3)+ c(CO32-)
D.c(Na+) + c(H+)== c(ClO-)+ c(HCO3-) + 2c(CO32-)
E.c(HClO) + c(H+)+ c(H2CO3)== c(OH-) + c(CO32-)
(4)写出少量的CO2通入NaClO溶液中的化学方程式 。
(5)0.1mol/L的酒石酸溶液与pH=13的NaOH溶液等体积混合,所得溶液的pH为6,则c(HC4H4O6-)+2 c(C4H4O62-)= 。(用准确的数值表示)
参考答案:(1) e c d b a (2)2.85(2分)(3)BC E
(4) CO2+ NaClO+ H2O= NaHCO3+ HClO
(5)(0.05+10-6-10-8)mol/L 或0.05000099 mol/L
本题解析:(1)分析题给电离平衡常数知,酸性:HC4H4O6―>CH3COOH> H2CO3>HClO> HCO3―,根据盐类水解规律:形成盐的酸根对应酸越弱,该盐的水解程度越大,同浓度溶液的碱性越强,PH越大,可知,物质的量浓度相同这五种盐溶液的PH:Na2CO3>NaClO >NaHCO3>CH3COONa> Na2C4H4O6,则pH相同的五种盐溶液的物质的量浓度:Na2CO3<NaClO <NaHCO3<CH3COONa< Na2C4H4O6,由大到小的顺序是e c d b a;(2)设0.1mol/L的CH3COOH溶液中氢离子浓度为x,代入醋酸的电离常数表达式得:x2/0.1=2.0×10-5,解得x=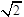 ×10-3,PH=2.85;(3)根据题给信息知,将0.1mol/L的次氯酸溶液与0.1mol/L的碳酸钠溶液等体积混合,发生的反应为:
×10-3,PH=2.85;(3)根据题给信息知,将0.1mol/L的次氯酸溶液与0.1mol/L的碳酸钠溶液等体积混合,发生的反应为:
HClO+ Na2CO3= NaClO+ NaHCO3,所得溶液为浓度均为0.05mol/L的NaClO和 NaHCO3的混合液,A、ClO-的水解程度大于HCO3-,则c(HCO3-) >c(ClO-) ,错误;B、c(Na+) > c(HCO3-) >c(ClO-) > c(H+),正确;C、根据物料守恒知,c(Na+)="c(HClO)" +c(ClO-)+ c(HCO3-) + c(H2CO3)+ c(CO32-),正确;D、根据电荷守恒知,c(Na+) + c(H+)= c(ClO-)+ c(HCO3-) + 2c(CO32-)+ c(OH-),错误;E、根据物料守恒和电荷守恒知,c(HClO) + c(H+)+ c(H2CO3)= c(OH-) + c(CO32-),正确;选BCE;(4)根据题意知H2CO3>HClO> HCO3―,少量的CO2通入NaClO溶液中的化学方程式为CO2+ NaClO+ H2O= NaHCO3+ HClO;(5)0.1mol/L的酒石酸溶液与pH=13的NaOH溶液等体积混合,所得溶液为0.05mol/L的NaHC4H4O6,根据电荷守恒式可知,c(HC4H4O6-)+2 c(C4H4O62-)= c(Na+) + c(H+) ―c(OH-)= (0.05+10-6-10-8)mol/L ="0.05000099" mol/L。
考点:考查电解质溶液,涉及弱电解质的电离和盐类的水解。
本题难度:困难
2、选择题 下列物质中,属于弱电解质的是(?)
A.氨水
B.冰醋酸
C.酒精
D.硫酸钡
参考答案:B
本题解析:电解质是在水溶液中或熔化状态下能够导电的化合物。弱电解质是在水溶液中只有部分电离产生离子的电解质。A.氨水是混合物。错误。B.冰醋酸在水分子的作用下,部分发生电离:CH3COOH CH3COO-+H+。还存在着电解质分子。是弱电解质。正确。C.酒精是非电解质。D.硫酸钡尽管难溶于水,但是溶于水的完全电离,所以是强电解质。错误。
CH3COO-+H+。还存在着电解质分子。是弱电解质。正确。C.酒精是非电解质。D.硫酸钡尽管难溶于水,但是溶于水的完全电离,所以是强电解质。错误。
本题难度:一般
3、选择题 室温下向10 mL pH = 3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中C(CH3COO-)/C(CH3COOH).c(OH-)不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH = 11的NaOH溶液,混合液pH=7
参考答案:B
本题解析:醋酸属于弱酸,加水稀释有利于醋酸的电离,所以醋酸的电离程度增大,同时溶液中导电粒子的数目会增大,由于溶液体积变化更大,所以溶液的酸性会降低,即c(H+)、c(CH3COO-)、c(CH3COOH)均会降低,因此选项A、C均不正确;由水的离子积常数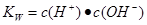 知
知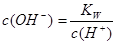 ,所以
,所以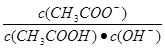 =
=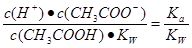 其中
其中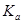 表示醋酸的电离平衡常数,由于水的离子积常数和醋酸的电离平衡常数均只与温度有关,所以选项B正确;pH=3的醋酸说明醋酸的浓度大于0.001mol/L,pH=11的NaOH溶液说明氢氧化钠的浓度等于0.001mol/L,因此加入等体积的pH=11的NaOH溶液时,醋酸会过量,溶液显酸性,D不正确,答案选B。
表示醋酸的电离平衡常数,由于水的离子积常数和醋酸的电离平衡常数均只与温度有关,所以选项B正确;pH=3的醋酸说明醋酸的浓度大于0.001mol/L,pH=11的NaOH溶液说明氢氧化钠的浓度等于0.001mol/L,因此加入等体积的pH=11的NaOH溶液时,醋酸会过量,溶液显酸性,D不正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。主要是考查学生对弱电解质电离平衡以及影响电离平衡因素的熟悉了解程度,有利于培养学生的逻辑推理能力和创新思维能力。明确温度与电离平衡常数的关系、溶液的pH与物质的量浓度的关系、稀释中溶液体积的变化与离子的物质的量的变化程度是解答本题的关键。
本题难度:一般
4、填空题 (8分)一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,
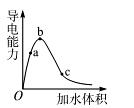
(1)O点导电能力为0的理由是?。
(2)a、b、c三点溶液的c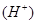 由小到大的顺序是?。
由小到大的顺序是?。
(3)a、b、c三点醋酸的电离程度最大的是?。
(4)要使c点c 增大,c
增大,c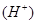 减少,可采取的措施是(至少写出三种方法)
减少,可采取的措施是(至少写出三种方法)
①?;②?;③?。
参考答案:(8分) (1) (1分)在O点醋酸未电离,无自由离子存在
(2) (2分)c<a<b? (3) (2分)c点
(4) (3分)加NaOH固体?加少量的碳酸钠固体?加入镁等金属?加醋酸钠固体等
本题解析:(1)冰醋酸在O点未能电离,不存在自由移动的离子,因此导电性未0。
(2)溶液的导电性越强,溶液中氢离子浓度越大,所以a、b、c三点溶液的c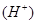 由小到大的顺序是c<a<b。
由小到大的顺序是c<a<b。
(3)醋酸是弱酸,存在电离平衡,稀释促进电离。所以a、b、c三点醋酸的电离程度最大的是c点。
(4)根据醋酸的电离方程式CH3COOH CH3COO-+H+可知,要使c点c
CH3COO-+H+可知,要使c点c 增大,c
增大,c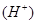 减少,可采取的措施有加NaOH固体或加少量的碳酸钠固体或加入镁等金属,或加醋酸钠固体等。
减少,可采取的措施有加NaOH固体或加少量的碳酸钠固体或加入镁等金属,或加醋酸钠固体等。
点评:在判断溶液的导电性时,需要注意的是,溶液的导电性只与溶液中离子浓度大小和离子所带电荷数有关系,离子浓度越大,电荷数越多,溶液的导电性越强,据此可以进行有关判断。
本题难度:一般
5、简答题 水是我们熟悉的物质,正如同学们所知道的,水能“分裂”出一个质子而离解,此处打引号是由于分裂出来的质子不是以游离状态存在于真实的化学体系中,而是立即与另一水分子结合:H2O+H2O?H3O++OH-K1=c(H3O+)?c(OH-)/c(H2O)氢氧根离子可进一步离解:OH-+H2O?H3O++O2-K2=c(H3O+)?c(O2-)/c(OH-)
(1)计算25℃时K1的值.______
(2)已知25℃时K2=10-36,计算在多少体积的水里含有一个氧负离子?______.
参考答案:(1)25℃时,纯水中c(H3O+)?c(OH-)=Kw=10-14,c(H2O)=1000g18g/mol1L=55.6mol/L,K1=c(H3O+).c(OH-)c(H2O)=10-1455.6=1.8×10-16,故答案为:1.8×10-16;
(2)水中c(H3O+)=c(OH-),K2=c(H3O+).c(O2-)c(OH-)则c(O2-)=K2?c(OH-)/c(H3O+)=K2=10-36,
1L水中氧负离子的个数=6.02×1023×10-36=6.02×10-13,设xL水中含有一个氧负离子,则1:6.02×10-13=x:1,x=1.7×1012,
故答案为:1.7×1012L水中有一个氧负离子.
本题解析:
本题难度:一般