1、选择题 某温度下,在体积为5L的密闭容器中,充入1mol?A气体,发生如下可逆反应:2A(g)?B(g)+C(g);△H=+akJ?mol-1?(a>0),2min后反应达到平衡,A为0.4mol下列叙述中不正确的是( )
A.0~2?min时间内B物质的平均反应速率为0.03?mol/(L?min)
B.充分反应后,反应吸收的热量小于0.5a?kJ
C.达平衡后,保持温度和容器体积不变,再充入1?mol?A,平衡向正反应方向移动
D.若温度和容器体积不变,起始时充入B和C各0.5?mol,则达平衡时,n(A)等于0.4?mol
参考答案:A、平衡时A的物质的量为0.4mol,参加反应的A的物质的量为1mol-0.4mol=0.6mol,结合方程式可知生成B的物质的量为0.6mol×12=0.3mol,故v(B)=0.3mol5L2min=0.03mol/(L?min),故A正确;
B、平衡时A的物质的量为0.4mol,参加反应的A的物质的量为1mol-0.4mol=0.6mol,根据2A(g)?B(g)+C(g);△H=+akJ?mol-1?(a>0)可知,吸收的热量为akJ×0.6mol2mol=0.3akJ,故B错误;
C、达平衡后,保持温度和容器体积不变,再充入1mol?A,反应向正反应方向移动,等效为增大压强,该反应前后气体的物质的量不变,为等效平衡,平衡状态相同,故C正确;
D、温度和容器体积不变,起始时充入B和C各0.5?mol,按化学计量数转化到左边可得1molA,与原平衡为等效平衡,平衡时对应组分的物质的量相同,平衡时A的物质的量为0.4mol,故D正确;
故选B.
本题解析:
本题难度:简单
2、选择题 下列事实不能用勒沙特列原理解释的是
A.新制的氯水在光照条件下颜色变浅
B.加入催化剂有利于氨的氧化反应
C.实验室中常用排饱和食盐水的方法收集氯气
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
参考答案:B
本题解析:略
本题难度:一般
3、选择题 反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率υ(x)可表示为
4NO(g)+6H2O(g),在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率υ(x)可表示为
[? ]
A.υ(NH3)=0.010mol/(L・s)
B.υ(O2)=0.001mol/(L・s)
C.υ(NO)=0.0015mol/(L・s)
D.υ(H2O)=0.090mol/(L・min)
参考答案:D
本题解析:
本题难度:简单
4、选择题 关于可逆反应mA(g)+nB(g)  pC(g)+qD(g)及其图象的说法正确的是(?)
pC(g)+qD(g)及其图象的说法正确的是(?)
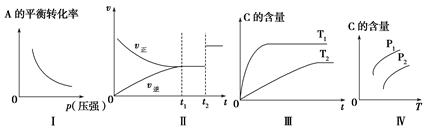
A.若图象为Ⅰ,则m+n>p+q
B.若图象为Ⅱ,则m+n=p+q,t2时刻改变的条件一定是使用催化剂
C.若图象为Ⅲ,则该可逆反应的ΔH<0
D.若图象为Ⅳ,且压强p1>压强p2,则该可逆反应的ΔH>0
参考答案:D
本题解析:若图象为Ⅰ,说明压强越大,A的转化率越低,则m+n<p+q,A错误;若图象为Ⅱ,且m+n=p+q,t2时刻改变的条件可能是增大压强,B错误;若图象为Ⅲ,根据温度越高,反应速率越快,达到平衡时间越短,则T1>T2,温度高时C的含量高,则ΔH>0,C错误;若图象为Ⅳ,且p1>p2,说明温度越高、压强越大,C的含量越高,则ΔH>0,m+n>p+q。
本题难度:一般
5、填空题 在密闭容器中,由一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内的分压与反应温度的关系如下图所示(已知气体的分压之比等于物质的量之比)。
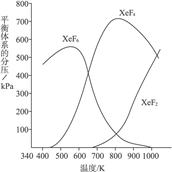
(1)420 K时,发生反应的化学方程式为:________________________;若反应中消耗1 mol Xe,则转移电子___________mol。
(2)600―800 K时,会发生反应:XeF6(g) XeF4(g)+F2(g),其反应热ΔH________0(填“>”“<”或“=”)。理由是_______________________________。
XeF4(g)+F2(g),其反应热ΔH________0(填“>”“<”或“=”)。理由是_______________________________。
(3)900 K时,容器中存在的组分有__________________________。
参考答案:(1)Xe+3F2====XeF6? 6
(2)>
随着温度的升高,XeF6(g) XeF4(g)+F2(g)平衡向右移动,根据温度升高平衡向吸热反应方向移动的原理,则该反应的ΔH>0。
XeF4(g)+F2(g)平衡向右移动,根据温度升高平衡向吸热反应方向移动的原理,则该反应的ΔH>0。
(3)XeF6、XeF4、XeF2、Xe、F2
本题解析:(1)由图象可知,在420 K时,平衡体系中无XeF4、XeF2生成(二者分压为零),只有生成物XeF6,此时反应的化学方程式为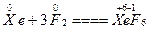 。若反应中消耗1 mol Xe时,则转移电子6 mol。
。若反应中消耗1 mol Xe时,则转移电子6 mol。
(2)在600―800 K时,反应XeF6(g) XeF4(g)+F2(g)达平衡后,随着温度的升高,XeF6不断减少,XeF4不断增多,上述平衡向右移动,说明正反应为吸热反应,该反应的ΔH>0。
XeF4(g)+F2(g)达平衡后,随着温度的升高,XeF6不断减少,XeF4不断增多,上述平衡向右移动,说明正反应为吸热反应,该反应的ΔH>0。
(3)由图象可知,在900 K时,平衡体系中三种生成物XeF6、XeF4、XeF2都存在,又因为是可逆反应,还应有反应物Xe、F2存在。
点评:本题以活泼性最强的非金属F2与稀有气体氙(Xe)反应,得到多种氟化物为载体,主要考查化学平衡、氧化还原反应、反应热ΔH等知识。题目以图象为情景设问,重点考查考生的观察能力和思维能力。综合性强,体现了以能力立意的思想。
本题难度:简单