1������� ����ӵ�صĹ㷺Ӧ��ʹ�����������Դ��Ϊ��Ҫ���⣮ij�о���С��ԷϾ�����ӵ���������ϣ�ͼ�м�Ʒ��ϣ��ɷ�ΪLiMn2O4��̼�ۺ�������������Դ�����о������ʵ���������£�
��֪��Li2SO4��LiOH��Li2CO3��303K�µ��ܽ�ȷֱ�Ϊ34.2g��12.7g��1.3g��

��1����������NaOH��Һ��ȡ֮ǰ��Ҫ���з����������Ŀ����______��
��2��д�����ɳ���X�����ӷ���ʽ______��
��3��д����Ӧ�ڵĻ�ѧ��Ӧ����ʽ______��
��4����Ӧ����ʵ�ʲ����в��ü��������Na2CO3���������Na2CO3��Һ����������Ŀ����______���������ˢ���������Li2CO3��������Һ�е���Ҫ�ɷ�Ϊ______����д��ѧʽ��
�ο��𰸣���һ���������ܽ�������������Һ�У�ע��LiMn2O4������ˮ���������ǻ��������ƣ�����Һ����Ҫ�ɷ֣��ڶ����������ǻ����������������̼��Ӧ������������������̼�����ƵĹ��̣���������LiMn2O4�����Ի������ܱ������е���������������������ԭ��Ӧ���õ�����Һ�������ɵ�����ﮣ������й��������ᣬ���һ������̼����֮�����õ���Һ��Ҫ�ɷ�Ϊ�����ƣ�
��1��������ϣ����������������������Һ�ĽӴ�������ӿ췴Ӧ���ʣ�
�ʴ�Ϊ������Ӵ�������ӿ췴Ӧ���ʣ�
��2�����ǻ��������������������̼��Ӧ�ò�����Al��OH��3������̼�����ƣ�
�������ӷ���ʽΪ��CO2+AlO2-+2H2O=Al��OH��3��+HCO3-��
�ʴ�Ϊ��CO2+AlO2-+2H2O=Al��OH��3��+HCO3-��
��3�������Ի����£�LiMn2O4�ܱ������е��������������ɶ������̡�����﮺�ˮ�����Ի�ѧ����ʽΪ��
4LiMn2O4+2H2SO4+O2=8MnO2+2Li2SO4+2H2O��
�ʴ�Ϊ��4?LiMn2O4+2?H2SO4+O2=8MnO2+2?Li2SO4+2H2O��
��4��̼������Һ�к���ˮ��������̼��﮵��ܽ⣬��ʹ��Һ�е�����ӳ�������ȫ��������̼���ƹ��岻��̼������Һ��ͨ���������֪�����������Һ�е���Ҫ�ɷ�Ϊ�����ƣ�
�ʴ�Ϊ��ʹ��Һ�е�Li+������ȫ������Li2CO3���ܽ⣬Na2SO4��
���������
�����Ѷȣ�һ��
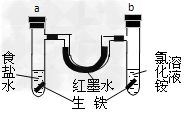
2��ѡ���� ��ͼװ���У�U����Ϊ��īˮ��a��b�Թ��зֱ�ʢ��ʳ��ˮ���Ȼ����Һ�������������飬����һ��ʱ�䡣�����й������������
[? ]
A��a�з�����������ʴ��b�з��������ⸯʴ
B�����Թ��и�����Ӧ���ǣ�Fe?�C?2e��=?Fe2��
C����������̼��ԭ�������
D����īˮ��һ��ʱ�������Һ���Ϊ����Ҹ�
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3��ѡ���� ����ͼ��ʾװ�ý���ʵ�飨����C1��C2����ʯī�缫��������˵������ȷ����?
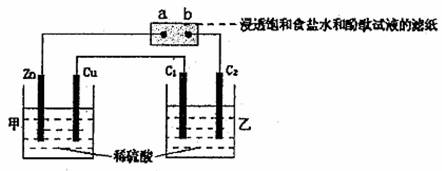
A����ͨ��״���£�Zn������3.25gʱ��C2���Ϸų��������ԼΪ1.12L
B������b�㸽���Ժ�ɫ
C������ͬ�����£�C1��C2�缫����������������Ϊ2��1
D���ҳ���Һ��pH��С
�ο��𰸣�D
�����������װ��ͼ֪���׳��������ϲ�ͬ��ZnΪ���ý��������Ϊԭ��أ�ZnΪ������CuΪ��������a��C2Ϊ���ص�������a��������졣B����b��C1Ϊ�������ҳ�ʵ���ǵ��ˮ����C1����O2��C2����H2���������Ϊ1��2��C��������ˮ����⣬C(H2SO4)����,PH��С��ѡD��ͨ��״���������Ħ���������22.4L/mol,A����
�����Ѷȣ�һ��
4������� �����˵�����δ��ʱϴ�������ñ����ʴ�����ֺ��ɫ��ߣ���ش�
��1����������ʴ��______��ʴ������⡱������������
��2��д��������ʴ�����ĵ缫��Ӧʽ��______��
�ο��𰸣���1����������������£���������������ʴ���ʴ�Ϊ��������
��2������̼�͵������Һ����ԭ��أ�̼�������������������õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ��2H2O+O2+4e-=4OH-���ʴ�Ϊ��2H2O+O2+4e-=4OH-��
���������
�����Ѷȣ�һ��
5������� ��9�֣���Ҫ�����ͼ���������б�Ҫ�����Ӳ���գ�
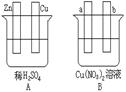
��1����Aͼ�У�ʹͭƬ��ðH2���ݡ�����Ա�Ҫ���ӣ������Ӻ��װ�ý�?���缫��Ӧʽ��
п�壺?��ͭ�壺?��
��2����Bͼ�У�a�� b����ʯī�缫��ʹa������ͭ����b������?�����Ա�Ҫ�����Ӻ缫��Ӧʽ��a����??b����?������һ��ʱ���ֹͣ��Ӧ�����һ������?����Һ�ָܻ�������ǰ��ȫһ�¡�
�ο��𰸣���1�� ?ԭ���?��п�壺Zn-2e- =Zn2��ͭ�壺2H����2e-��H2��
?ԭ���?��п�壺Zn-2e- =Zn2��ͭ�壺2H����2e-��H2��
��2��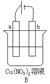 O2�����أ�a����Cu2����2e- =Cu��b����4OH�D�D4e����O2����2H2O��CuO��ÿ��1�֣�δ�������ߴ�������۷֣�
O2�����أ�a����Cu2����2e- =Cu��b����4OH�D�D4e����O2����2H2O��CuO��ÿ��1�֣�δ�������ߴ�������۷֣�
�����������1��ҪʹͭƬ�ϲ������ݣ���Ӧ�ù���ԭ��أ�п�Ǹ�����ʧȥ���ӡ�ͭ����������Һ�е��������������õ����ӣ��缫��ӦʽΪп�壺Zn-2e- =Zn2��ͭ�壺2H����2e-��H2����
��2��ʹa������ͭ��Ӧ�ù��ɵ��أ�����a��������������b����������b��OH���ŵ磬�����������缫��Ӧʽ�ֱ���a����Cu2����2e- =Cu��b����4OH�D�D4e����O2����2H2O�����ڴ���Һ�м��ٵ���ͭ������������Ӧ�ü�������ͭ���ָܻ������ǰ��״̬��
�����Ѷȣ���