1、填空题 (6分)利用氧化还原反应原理配平以下化学方程式,并:
FeSO4 + KNO3 + H2SO4 === K2SO4 + Fe2(SO4)3 + NO↑+ H2O
(1)标出电子转移的方向和数目
(2)当电子转移了0.3mol时,有?g氧化剂参加反应
2、选择题 关于反应3Cl2 + 6KOH 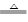 ?KClO3 + 5KCl + 3H2O,以下说法正确的是
?KClO3 + 5KCl + 3H2O,以下说法正确的是
A.KOH既不是氧化剂,又不是还原剂
B.Cl2是氧化剂,KOH是还原剂
C.3mol氯气参加反应转移6 mol电子
D.被氧化的氯元素的质量为被还原的氯元素质量的5倍
3、选择题 xR2++yH++O2?mR3++2H2O中,对m和R3+判断正确的是
A.m=4,R2+是氧化剂
B.2m=y,R3+是氧化剂
C.m=4,R3+是氧化产物
D.m=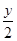 ,R3+是还原剂
,R3+是还原剂
4、选择题 已知锌溶于稀硝酸中可发生如下反应:4Zn+10HNO3==4Zn(NO3)2+N2O↑+5H2O,该反应中被还原的硝酸与未被还原的硝酸的质量比是
A.2∶5
B.1∶4
C.4∶1
D.5∶1
5、填空题 (1)在标准状况下,3.55g氯气的体积是______L,将其与氢气完全化合需氢气的物质的量是______mol,将生成的气体制成100mL溶液,溶质的物质的量浓度是______mol?L-1,将此溶液取出20mL加蒸馏水稀释成500mL溶液,此稀稀后的溶液中溶质的物质的量浓度是______mol?L-1.
(2)写出下列反应的化学方程式:
①镁在二氧化碳中燃烧反应:______.
②实验室用二氧化锰与浓盐酸反应制取氯气:______.
③金属铜与浓硫酸加热反应:______.
(3)白磷(P4)是一种常见的晶体,可用于制备较纯的磷酸.已知白磷和氯酸溶液可发生如下反应:
______P4+______HClO3+______=______HCl+______H3PO4
配平并完成上述反应方程式,该反应的氧化剂是______;若有1mol?P4反应,则有______mol电子转移.