1、填空题 在一定温度下,将2molA和2molB两种气体混合放入体积为2L的密闭刚性容器中,发生如下反应: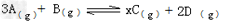 ?
?
2min末反应达到平衡,生成0.8molD,并测得C的浓度为0.4mol/L
请回答: ?
(1)x的值为_______?
(2)A的转化率为α(A)%=______________ ?
(3)此温度下该反应的平衡常数K=___________
参考答案:(1)x=2?
(2)α(A)%=60%
(3)0.5
本题解析:
本题难度:一般
2、计算题 在某温度下,将H2和I2各0. 10 mol的气态混合物充入10L的密闭容器中,充分反应达到平衡后,测得c(H2)= 0.008 0mol・L-1。
(1)求该反应的平衡常数。
(2)在上述温度下,该容器中若通入H2和I2蒸气各0. 20 mol,试求达到化学平衡状态时各物质的浓度。
参考答案:(1)平衡常数为0.25。
(2)c( H2)=c(I2)=0.016 mol/L,c( HI)=0.008 0mol/L。
本题解析:
本题难度:一般
3、填空题 (10分)接触法制硫酸的核心反应是2SO2(g)? + O2(g) 2SO3(g) ;△H<0。在2L恒容的密闭容器中,加入3molSO3(g)和lmol氧气,在一定温度下使其反应,反应至4min时,氧气的浓度为0.6mol・L-1,当反应到8min时,反应到达平衡,此时c(SO3)=a mol・L-1。
2SO3(g) ;△H<0。在2L恒容的密闭容器中,加入3molSO3(g)和lmol氧气,在一定温度下使其反应,反应至4min时,氧气的浓度为0.6mol・L-1,当反应到8min时,反应到达平衡,此时c(SO3)=a mol・L-1。
(1) 0min~4min内生成O2平均速率v(O2)=?;如果0min~4min内SO3生成速率平均为x,4min~8min内SO3生成速率平均为y,8min~10min内SO3生成速率平均为z(其它条件不变,且忽略反应中温度变化),则x、y、z大小关系为______________。
(2) 达到平衡时c(O2)=c(SO2),则a=?mol・L-1;如果此时在平衡体系中加入0.5molN2,则SO2在混合气中所占的体积分数____________(填“增大”、“减小”或“不变”)
(3) 若起始时n(SO3)、n(SO2)、n(O2)(/mol)分别按下列4组数据投料,相同温度下达到平衡时,三氧化硫浓度大于a mol・L-1的是?。
A.1、2、2
B.3、1.5、1
C.3、0、0
D.0、6、5
参考答案:(每空2分)(1)0.025mol・L-1・min-1?x<y<z(2)a=0.5?减小
(3) B? D
本题解析:略
本题难度:简单
4、选择题 在一体积不变的密闭容器中发生如下化学反应:2A(g) B(g)+C(g)。当物质A的起始浓度为1.0 mol・L-1、物质B、C的起始浓度为0时,物质A的浓度、转化率以及物质B的浓度随反应时间的变化如下列各图所示:
B(g)+C(g)。当物质A的起始浓度为1.0 mol・L-1、物质B、C的起始浓度为0时,物质A的浓度、转化率以及物质B的浓度随反应时间的变化如下列各图所示:
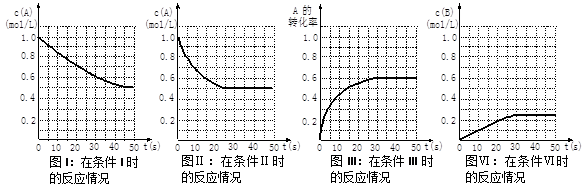
则下列有关说法中正确的是
A.条件I、条件II时的反应温度不同,压强相同
B.条件I时可能未使用催化剂,条件II时可能使用了催化剂
C.条件III时的平衡混合物中,物质C的浓度等于0.6 mol・L-1
D.条件IV和条件II相比较,条件IV时可能缩小了容器体积
参考答案:B
本题解析:根据图像可知图I、图II平衡时A的浓度是相同的,但达到平衡的时间不同,又因为反应前后体积不变,这说明反应温度相同,压强不相同或使用了催化剂,A不正确,B正确;条件III时A的平衡转化率是0.6,所以生成C的浓度是0.3mol/L,C不正确;条件IV和条件II相比较,平衡时的状态是相同的,且达到平衡的时间也是相同的,所以D不正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生的逻辑推理能力,提高学生的学习效率和学科素养。
本题难度:简单
5、选择题 在容积可变的密闭容器中,10 mol N2和30 mol H?2在一定条件下反应,达到平衡时,H2的转化率为25%,则平衡时氨气的物质的量为( )
A.2.5 mol
B.4.5 mol
C.5mol
D.7.5 mol
参考答案:C
本题解析:合成氨反应的方程式为:3H2 + N2?2NH3;H2的转化率为25%,即H2的的物质的量变化为:30 mol×25%="7.5" mol;根据反应过程中,变化的量之比=化学计量数之比,即平衡时氨气的物质的量为5mol。
本题难度:简单