1、填空题 生锈的铁钉与过量的盐酸发生反应的离子方程式为____________。
2、选择题 某含铬[Cr2O72-] 废水用硫酸亚铁铵[FeSO4・(NH4)2 SO4・6H2O]处理,反应中铁元素和铬元素完全转化为沉淀.该沉淀干燥后得到n molFeO・FeyCrxO3.不考虑处理过程中的实际损耗,下列叙述错误的是?(?)
A.消耗硫酸亚铁铵的物质量为n(2-x)mol
B.处理废水中Cr2O72-的物质量为mol
C.反应中发生转移的电子数为3nx mol
D.在FeO・FeyCrxO3中3x=y
3、选择题 向一定量的Fe、FeO、Fe2O3混合物中加入100 mL 1 mol/L盐酸,恰好使混合物完全溶解,放出224 mL(标准状况下)的气体,在所得溶液中加入KSCN溶液,无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,可得到铁的质量是(?)
A.11.2g
B.5.6g
C.2.8g
D.无法计算
4、实验题 工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为:
2FeSO4 ="===" Fe2O3 +SO2↑+SO3↑?为检验FeSO4高温分解的产物,进行如下实验:
①取少量FeSO4高温分解得到的固体,加一定量稀盐酸溶解,向该溶液中加入适量的KSCN溶液,观察溶液颜色的变化以检验Fe3+是否存在。
②将FeSO4高温分解产生的气体通入右图所示的装置中,以检验产生的气体中是否含有SO2和SO3。请回答以下问题:

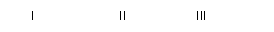
(1)写出用KSCN检验Fe3+的离子方程式?。
(2)装置I中试剂为氯化钡溶液,进行操作②时氯化钡溶液中有白色沉淀产生。甲同学说,这个白色沉淀可能是BaSO4和BaSO3的混合物;乙同学说,这个白色沉淀是BaSO4;丙同学说,这个白色沉淀是BaSO3。请你设计一个简单的实验帮他们加以鉴别。
?
你认为上述哪一位同学的观点正确??
(3)装置II中试剂为品红溶液,其作用是?,品红溶液中可观察到现象是?。
(4)装置III中试剂为NaOH溶液,其目的是?。
5、实验题 (10分)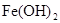 由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用图装置使用
由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用图装置使用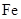 ,
,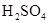 (稀),NaOH溶液可在还原性气氛中制取
(稀),NaOH溶液可在还原性气氛中制取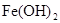 白色沉淀,且较长时间内不变色,其中C为弹簧夹,则锥形瓶A中应加入的药品为________,锥形瓶B中应加入的药品为________.容器A中的反应开始后,请设计后续操作步骤完成的制备,并说明每步操作理由和现象.
白色沉淀,且较长时间内不变色,其中C为弹簧夹,则锥形瓶A中应加入的药品为________,锥形瓶B中应加入的药品为________.容器A中的反应开始后,请设计后续操作步骤完成的制备,并说明每步操作理由和现象.