1、选择题 下列四种盐酸溶液,均能跟锌片反应,其中最初反应速率最快的是
[? ]
A.10℃ 20mL 3mol/L的盐酸溶液
B.20℃ 30mL 2mol/L的盐酸溶液
C.20℃ 20mL 2mol/L的盐酸溶液
D.20℃ 10mL 4mol/L的盐酸溶液
参考答案:D
本题解析:
本题难度:一般
2、选择题 在密闭容器中充入一定量的NO2,发生反应2NO2(g) N2O4(g)?△H=-57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
N2O4(g)?△H=-57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
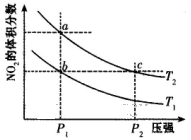
A.a、c两点的反应速率:a>c
B.a、b两点的转化率:a<b
C.a、c两点气体的颜色:a深,c浅
D.由a点到b点,可以用加热的方法
参考答案:B
本题解析:A、a、c两点所在的温度相同,但c点的压强高于a点的压强。压强高,反应速率快,因此反应速率为a<c,A不正确;B、a点NO2的体积分数大于b点NO2的体积分数,这说明a、b两点的转化率是a<b,B正确;C、c点的压强高于a点的压强,压强高,容器的容积小,N2O4的浓度大,所以颜色深浅是a浅,c深,C不正确;D、正方应是放热反应,由a点到b点,NO2的体积分数减小,说明平衡向正反应方向移动,因此不能用加热的方法,应该是降低温度,D不正确,答案选B。
本题难度:一般
3、选择题 下列说法正确的是
[? ]
A.增大反应物浓度,可增大单位体积内活化分子百分数,从而使有效碰撞次数增大
B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
参考答案:C
本题解析:
本题难度:一般
4、选择题 在一定温度下的定容密闭容器中,下列说法能表明反应:A(s)+2B(g) 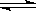 C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是
A.混合气体的压强不变
B.消耗2molB的同时生成1molC
C.混合气体的相对分子质量不变
D.气体的总物质的量不变
参考答案:C
本题解析:反应前后体积不变,即气体的总物质的量不变,压强恒定。消耗2molB的同时一定生成1molC,所以不能说明。混合气体的相对分子质量是混合气的质量和混合气的物质的量的比值,物质的量不变,但质量是变化的,所以C可以说明。答案是C
本题难度:简单
5、选择题 可逆反应:mA(g)+nB(g) pC(g)+gD(g)的v-t图象如图甲所示;若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图象如图乙所示。现有下列叙述:
pC(g)+gD(g)的v-t图象如图甲所示;若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图象如图乙所示。现有下列叙述:
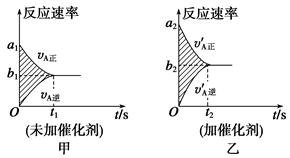
①a1=a2②a1<a2③b1=b2④b1<b2⑤t1>t2 ⑥t1=t2⑦甲图与乙图中阴影部分的面积相等
⑧图乙中阴影部分面积更大。则以上所述各项正确的组合为( )
A.②④⑥⑧
B.②④⑤⑦
C.②③⑤⑦
D.②③⑥⑧