1、选择题 下列说法错误的是
A.作半导体材料的元素大多数位于周期表中金属和非金属的交界处
B.农药中常含有的元素通常在元素周期表的右上方区域内
C.作催化剂材料的元素通常在元素周期表的左下方区域内
D.在周期表过渡元素中可寻找到耐高温和耐腐蚀的合金材料
参考答案:C
本题解析:元素周期表沿金属和非金属的交界处划了一条线,即金属与非金属的分界线,在此线附近寻找作半导体材料,在元素周期表的右上方区域内的非金属元素中寻找作农药的元素,在周期表过渡元素中可寻找到耐高温和耐腐蚀的合金材料及催化剂材料,在元素周期表的中间区域内,在元素周期表的左下方区域内是一些典型的金属元素.
本题难度:简单
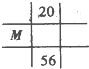
2、选择题 下列各图为元素周期表的一部分,表中的数字为原子序数,其中M为37的是( )
A.

B.

C.
D.
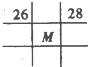
参考答案:M的原子序数为37,位于周期表中第五周期第ⅠA族.
A、17号、53号元素为第ⅦA族元素,图中M为稀有气体Kr,故A错误;
B、19号,55号元素处于第ⅠA族,M应处于二者之间,故B错误;
C、20号,56号元素处于第ⅡA族.20号元素为钙元素,处于第四周期第ⅡA族,M位置正确,故C正确;
D、26号、28号元素为第Ⅷ族元素,图中M处于第Ⅷ族,故D错误.
故选:C.
本题解析:
本题难度:简单
3、选择题 某元素的原子最外层有2个电子,则该元素是
[? ]
A.金属元素?
B.稀有气体元素?
C.第ⅡA族元素? ?
D.以上叙述都可能
参考答案:D
本题解析:
本题难度:简单
4、选择题 下列叙述中,甲金属一定比乙金属活泼性强的是( )
A.甲原子电子层数比乙原子的电子层数多
B.在甲乙两种金属和盐酸构成的原电池中,甲作正极,乙作负极
C.1mol甲和乙分别与足量的盐酸反应,产生H2的量:甲>乙
D.常温时,甲能从水中置换出氢,而乙不能
参考答案:A、如金属不位于同一主族,则不能根据电子层数的多少来判断金属的活泼性强弱,故A错误;
B、在甲乙两种金属和盐酸构成的原电池中,甲作正极,乙作负极,说明乙活泼,故B错误;
C、产生氢气的多少取决于金属失去电子数的多少,与金属的活泼性无关,故C错误;
D、金属的活泼性越强,越易与水反应,故D正确.
故选D.
本题解析:
本题难度:简单
5、填空题 A.B.C.D 4种元素,A元素所处的周期数.主族序数.原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1)B元素的名称________;B在周期表中的位置________;
(2)A.B形成的化合物的电子式_______;
(3)C的最高价氧化物的化学式________;
(4)D的最高价氧化物对应的水化物的化学式________.
参考答案:(1)氮;第二周期,VA族
(2)
(3)SO3
(4)KOH
本题解析:
本题难度:一般