1������� ����úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ��ú����ҵ��
��1����ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��C��s��+H2O��g��

CO��g��+H2��g����H=+131.3kJ?mol-1��
�÷�Ӧ�ڳ�����______�Է����У���ܡ��롰���ܡ�������һ���Ϊ2L���ܱ������У�����1molC��2mol?H2O��g������ƽ��ʱH2O��ת����Ϊ20%��������ʱ��ƽ�ⳣ��______
��2��Ŀǰ��ҵ����һ�ַ�������CO��H2��Ӧ�������״���
| ��ѧ�� | C-O | C-H | H-H | C��O | O-H
|
| ���� kg/mol-1 | 358 | 413 | 436 | 1072 | 463
|
��֪������̬�״���CO���溬C��O����д���÷�Ӧ���Ȼ�ѧ����ʽΪ______
��3�������Ǻϳɰ�����Ҫԭ�ϣ��ϳɰ���Ӧ���Ȼ�ѧ����ʽ���£�
N2��g��+3H2��g��

2NH3��g����H=-92.4kJ/mol
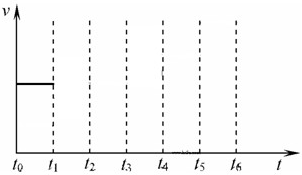
��һ�������������У����ϳɰ���Ӧ�ﵽƽ�����t1ʱ�����¶ȣ�t2���´ﵽƽ�⣬t3ʱ���뵪����t4ʱ���´ﵽƽ�⣬t5ʱ��ȥһ���ֲ��t6ʱ�ִﵽƽ�⣬��������ķ�Ӧ������ʱ���ϵͼ�л���t1��t5�淴Ӧ���ʡ�t5��t6����Ӧ���ʵı仯�����
��4����������������ȼ�ϵ�أ���������Ҳ���ԣ�������ѧ�ҳɹ�������Яʽ����������ȼ�ϵ�أ����Ա�������Ϊȼ�ϣ�һ��ͨ���������һ��ͨ��������壬������ǹ�̬�����������״̬���ܴ���O2-����ͨ����ĵ缫�����ĵ缫��ӦΪ______
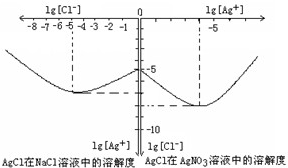
������ﲢ�Ǿ��Բ��ܣ�����ˮ�����ֲ�ͬ����Һ���ܽ��������ͬ��ͬ����ЧӦ���������γɵȶ���ʹ��������ܽ�������ı䣮��֪AgCl+Cl-=[AgCl2]-����ͼ��ij�¶���AgCl��NaCl��Һ�е��ܽ��������������Ϣ��֪��
��1����ͼ֪���¶���AgCl���ܶȻ�����Ϊ______��
��2��AgCl��NaCl��Һ�е��ܽ������ͼ��ʾ������ȱ�С����ԭ���ǣ�______��
�ο��𰸣���1���÷�ӦΪ������������ķ�Ӧ���ɡ�G=��H-T��S����G��0��Ӧ���Է����У���֪�÷�Ӧ�ڸ���ʱ�����Է����У������������Է����У�
�μӷ�Ӧ��ˮ�����ʵ���Ϊ2mol��20%=0.4mol����
���ڷ�Ӧ? C��s��+H2O��g��

CO��g��+H2��g����
��ʼ��mol����1? 2? 0?0
�仯��mol����0.4?0.4?0.4
ƽ�⣨mol����1.6?0.4?0.4
����ƽ��ʱH2O��Ũ��Ϊ1.6mol2L=0.8mol/L��CO��H2��Ũ��Ϊ0.4mol2L=0.2mol/L��
����ƽ�ⳣ��k=c(CO)?c(H2)c(H2O)=0.2��0.20.8=0.05��
�ʴ�Ϊ�������Է����У�0.05��
��2������CO��g��+2H2��g��=CH3OH��g������Ӧ�ȡ�H=1072KJ/mol+2��436KJ/mol-��413KJ/mol��3+358KJ/mol+463KJ/mol?��=-116?KJ/mol��
���Ը÷�Ӧ���Ȼ�ѧ����ʽΪCO��g��+2H2��g��=CH3OH��g����H=-116?KJ/mol��
�ʴ�Ϊ��CO��g��+2H2��g��=CH3OH��g����H=-116?KJ/mol��
��3����t1ʱ�����¶ȣ����淴Ӧ���ʶ�����ӦΪ���ȷ�Ӧ�������¶�ƽ�����淴Ӧ�ƶ����淴Ӧ��������࣬t2���´ﵽƽ�⣬ƽ��ʱ���ʱ�ԭ���ߣ�
t3ʱ���뵪����ƽ��������Ӧ�ƶ��������ﰱ����Ũ�������淴Ӧ��������t4ʱ���´ﵽƽ�⣻
t5ʱ��ȥһ���ֲ������Ũ�Ƚ��ͣ�ƽ��������Ӧ�ƶ�����Ӧ��Ũ�Ƚ��ͣ�����Ӧ���ʽ��ͣ�t6ʱ�ִﵽƽ�⣮
�ݴ���ͼΪ
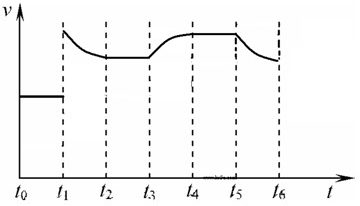
���ʴ�Ϊ��

��
��4����������������Ӧ�����Ա���Ӧ�ڸ�����ͨ�룬����ʧȥ�����������ӷ�Ӧ�����ɶ�����̼��ˮ���缫��ӦʽΪC3H8+10O2--20e-=3CO2+4H2O��
�ʴ�Ϊ��C3H8+10O2--20e-=3CO2+4H2O��
��1����ͼ��֪AgCl���ܶȻ�Ksp��AgCl��=c��Ag+��?c��Cl-��=10-5��10-7=10-12���ʴ�Ϊ��10-12��
��2����ʼCl-������AgCl���ܽ⣬����Ag+Ũ�ȱ�С�ˣ���Cl-Ũ������ʹAgCl�γ�[AgCl2]-����AgCl+Cl-=[AgCl2]-������Ag+Ũ���ֱ���ˣ�
�ʴ�Ϊ����ʼCl-������AgCl���ܽ⣬����Ag+Ũ�ȱ�С�ˣ���Cl-Ũ������ʹAgCl�γ�[AgCl2]-����AgCl+Cl-=[AgCl2]-������Ag+Ũ���ֱ���ˣ�
���������
�����Ѷȣ���
2������� ��ˮAlCl3�������л��ϳɵĴ�����ʳƷ���ɼ��ȣ���ҵ�Ʊ���ˮAlCl3���������£�
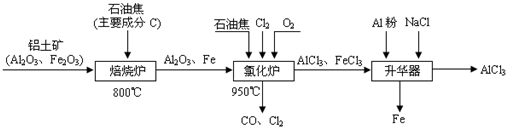
��1����֪��C��s��+
O2��g���TCO��g����H=-110.5kJ/mol��2Fe��s��+O2��g���TFe2O3��s����H=-822.1kJ/mol
��д��C��ԭFe2O3����CO���Ȼ�ѧ����ʽ______��
��2����Ӧ2CO+O2
2CO2��ƽ�ⳣ��ΪK1����Ӧ4Fe+3O2

2Fe2O3��ƽ�ⳣ��K2����Ӧ3CO+Fe2O3

2Fe+3CO2��ƽ�ⳣ��K��K1��K2�Ĺ�ϵʽ______��
��3�������£��������ܸ�̼�������з�Ӧ��
��Fe2O3+3C2Fe+3CO?��Fe2O3+3CO2Fe+3CO2����Ӧ������������CO2��CO������ȡֵ��Χ��______��
��4���Ȼ�¯�����ɵ����壬ͨ���ü��Ե�����������Һ�����գ��������ӷ���ʽ��������������Һ�ʼ��Ե�ԭ��______��
��5���Ȼ�¯�з�����3Cl2��g��+3C��s��+Al2O3��s��

2AlCl3��g��+3CO��g����H��0������߽��������Ȼ�Ч�������ɲ�ȡ�Ĵ�ʩ��______������ţ���
������C����?�ڶ�ͨ��Cl2�������¶�?�����߲���AlCl3��g��?��ʹ�ú��ʵĴ�����ҵ�ϻ����������Ȼ�¯��ͨ��O2�ķ�������Ŀ����______��
��6������������һ��涨����Һ��ij�������ʵ���Ũ�ȵ���1.0��10-5mol/Lʱ������Ϊ�ѳ�����ȫ������һ��Ũ�ȵ�AlCl3��FeCl3�Ļ����Һ����μ��백ˮ����Fe3+��ȫ����ʱ���ⶨc��Al3+��=0.2mol/L����ʱ���ó�����______����ǡ�������Al��OH��3������֪��Ksp[Fe��OH��3]=4.0��10-38��Ksp[Al��OH��3]=1.1��10-33����
�ο��𰸣���1��C��ԭFe2O3����CO���Ȼ�ѧ����ʽ��3C��s��+Fe2O3��s���T3CO��g��+2Fe��s������H
�ɸ�˹���ɣ�����һ������һ���Ȼ�ѧ����ʽ����3����ȥ�ڶ����Ȼ�ѧ����ʽ�����ø��Ȼ�ѧ����ʽ��
��Ӧ�ȡ�H=3����-110.5kJ/mol��-��-822.1kJ/mol��=+490.6kJ/mol��
����C��ԭFe2O3����CO���Ȼ�ѧ����ʽΪ��3C��s��+Fe2O3��s���T3CO��g��+2Fe��s����H=+490.6kJ/mol��
��2����Ӧ2CO+O2

2CO2��ƽ�ⳣ��ΪK1=c2(CO2)?c2(CO)?c(O2)��
��Ӧ4Fe+3O2

2Fe2O3��ƽ�ⳣ��K2=c2(Fe2O3)?c4(Fe)?c3(O2)?��
��Ӧ3CO+Fe2O3

2Fe+3CO2��ƽ�ⳣ��K=c3(CO2)?c2(Fe)c3(CO)?c(Fe2O3)?=
���������
�����Ѷȣ�һ��
3��ѡ���� �����й��Ȼ�ѧ����ʽ��������ȷ����
[? ]
A����20.0g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7kJ����������ϡ�����ϡNaOH��Һ��Ӧ���Ȼ�ѧ����ʽΪ��NaOH(aq) + CH3COOH(aq) = CH3COONa(aq) + H2O(l) �� ��H =��57.4kJ��mol-1
B����֪C��ʯī��s��= C�����ʯ��s������H>0����ʯī�Ƚ��ʯ�ȶ�
C����֪��Ӧ2H2(g) + O2(g) = 2H2O(l)����H=��571.6kJ��mol-1����H2��ȼ����Ϊ285.8kJ��mol-1
D����֪2C(s)+2O2(g)=2CO2(g) ��H1��2C(s)+O2(g)=2CO(g) ��H2�����H1>��H2?
�ο��𰸣�BC
���������
�����Ѷȣ���
4��ѡ���� ��298K��1.01��105Pa�£�12gʯī��24g������ȼ������Ӧ����ȫ���ģ���÷ų�x?kJ��x��0������������֪�ڸ������£�1molʯī��ȫȼ�շų�y?kJ��y��0������������ʯī��������Ӧ����CO���Ȼ�ѧ����ʽ������ȷ���ǣ�������
A��C��ʯī��s��+O2��g��=CO��g����H��298K��=-ykJ?mol-1
B��C��ʯī��s��+O2��g��=CO��g����H��298K��=-xkJ?mol-1
C��C��ʯī��s��+ O2��g��=CO��g����H��298K��=-��2x-y��kJ?mol-1
O2��g��=CO��g����H��298K��=-��2x-y��kJ?mol-1
D��2C��ʯī��s��+O2��g��=2CO��g����H��298K��=-��2x-y��kJ?mol-1
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� ����˵�����ʾ������ȷ����
[? ]
A����Ҫ���ȷ����ķ�Ӧ�����ȷ�Ӧ
B����ϡ��Һ�У�H��(aq)��OH��(aq)��H2O(l)����H����57.3kJ/mol��������0.5mol?H2SO4��Ũ�����뺬1molNaOH����Һ��ϣ��ų�����������57.3kJ
C����C(ʯī)��C(���ʯ)����H����1.73?kJ/mol����֪���ʯ��ʯī�ȶ�
D����101kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2(g)��O2(g)��2H2O(l)����H����285.8kJ/mol
�ο��𰸣�B
���������
�����Ѷȣ���