1、选择题 已知常温时红磷比白磷稳定,在下列反应中
P4(白磷,s)+5O2(g) =2P2O5(s) △H= -akJ/mol
4P(红磷,s)+5O2(g) =2P2O5(s) △H= -bkJ/mol
若a、b均大于零,则a和b的关系为
[? ]
A.a>b
B.a=b
C.a<b
D.无法确定
2、选择题 在CO跟O2的反应中,破坏1molCO中的化学键消耗的能量为A,破坏1molO=O键消耗的能量为B,形成1molC=O键释放的能量为C。则下列关系正确的是
A.2A+B>2C B.2A+B>4C C.2A + B < 2C D.2A + B < 4C
3、填空题 (8分)(1)已知2 mol氢气燃烧生成液态水时放出572 kJ热量,反应方程式是2H2(g)+O2(g)===2H2O(l) 请回答下列问题:
①该反应的生成物能量总和________(填“大于”、“小于”或“等于”)反应物能量总和。
②若2 mol氢气完全燃烧生成水蒸气,则放出的热量________(填“>”、“<”或“=”)572 kJ。
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g) 
4、填空题 CO2的固定和利用在降低温室气体排放中具有重要作用,从CO2加氢合成甲醇不仅可以有效缓解减排压力,还是其综合利用的一条新途径。CO2和H2在催化剂作用下能发生反应CO2+3H2 CH3OH+H2O,测得甲醇的理论产率与反应温度、压强的关系如图所示。请回答下列问题:
CH3OH+H2O,测得甲醇的理论产率与反应温度、压强的关系如图所示。请回答下列问题:
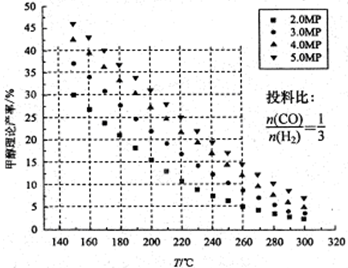
(1)提高甲醇产率的措施是 & #160; 。
(2)分析图中数据可知,在220 ℃、5MPa时,CO2的转化率为 ,再将温度降低至
140℃,压强减小至2MPa,化学反应速率将 (填“增大、减小 或 不变“ 下同),CO2的转化率将 。
(3)200℃时,将0.100molCO2和0.275molH2充入1L密闭容器中,在催化剂作用下反应达到平衡。若CO2的转化率为25%,则此温度下该反应的平衡常数K= 。(要求写出算式和计算结果)
(4)已知已知:CO的燃烧热△H=-283.0KJ/mol、2H2(g)+O2(g)=2H2O(g) △H=-483.6KJ/mol、
CO(g)+2H2(g)=CH3OH(g) △H=-90.1KJ/mol,写出CO2与H2合成甲醇的热化学方程式 。
5、选择题 下列热化学方程式书写正确的是( )
A.2SO2+O2 2SO3 ΔH=-196.6 kJ・mol-1
2SO3 ΔH=-196.6 kJ・mol-1
B.C(s)+O2(g)===CO2(g) ΔH=+393.5 kJ・mol-1
C.H2(g)+Cl2(g)===HCl(g) ΔH=-92.5 kJ・mol-1
D.H+(aq)+OH-(aq)===H2O(l) ΔH=+57.3 kJ