1������� ��6�֣��ܱ���ϵ�з������з�Ӧ��N2 + 3H2 ="===" 2NH3������ӦΪ���ȷ�Ӧ������ͼ��ijһʱ��η�Ӧ�����뷴Ӧ���̵����߹�ϵͼ��
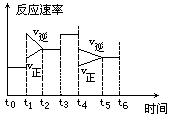
�ش��������⣺
��1������ƽ��״̬��ʱ�����_________________________________________________________
��2��t1��t3��t4ʱ�̣���ϵ�зֱ���ʲô���������˱仯��
t1��_______ ?t3��_______? t4��_________
��3������ʱ����У����İٷֺ�����ߵ���________
A��t 0~t1��
B��t2~t3
C��t3~t4
D��t5~t6
�ο��𰸣���1��t0��t1 ��t2��t3��t3��t����t5��t6
?��2��t1������? t3: �������? t4����ѹ?
��3��A
�����������
�����Ѷȣ���
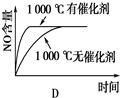
2��ѡ���� ��֪��4NH3 (g)��5O2(g) 4NO(g)��6H2O(g)��H����1025 kJ/mol������Ӧ����ʼ���ʵ�����ͬ�����й��ڸ÷�Ӧ��ʾ��ͼ����ȷ����
4NO(g)��6H2O(g)��H����1025 kJ/mol������Ӧ����ʼ���ʵ�����ͬ�����й��ڸ÷�Ӧ��ʾ��ͼ����ȷ����
 ?
? ?
? ?
?
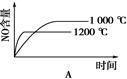
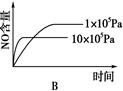
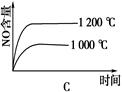
�ο��𰸣�C
������������ݷ�Ӧʽ��֪���÷�Ӧ���������ķ��ȵĿ��淴Ӧ�����Լ�Сѹǿ���¶�ƽ�ⶼ������Ӧ�����ƶ���NO�ĺ���������Ӧ���ʾ��ǽ��ͣ��ݴ˿�֪��ѡ��C���������⣬��ѡC��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ��������Ĺؼ������Ⲣ�����������������ԭ�����κ��ٽ��ͼ��;���ķ�Ӧʽ������ü��ɣ�����������ѧ����������������
�����Ѷȣ���
3��ѡ���� ������A��B�ֱ�Ϊ0.6mol��0.5mol����0.4L�ܱ������з�����Ӧ��3A+B mC+2D����5min��ﵽƽ�⣬��ʱCΪ0.2mol����֪�ڴ˷�Ӧʱ��D��ƽ����Ӧ����Ϊ0.1mol��L-1��min-1�����½�����ȷ����?��?��
mC+2D����5min��ﵽƽ�⣬��ʱCΪ0.2mol����֪�ڴ˷�Ӧʱ��D��ƽ����Ӧ����Ϊ0.1mol��L-1��min-1�����½�����ȷ����?��?��
A.mֵΪ3 ?
B.B��ת����Ϊ20%?
C.A��ƽ����Ӧ����Ϊ0.1mol��L-1��min-1?
D.ƽ��ʱ��Ӧ����������ʵ���Ϊ1mol
�ο��𰸣�B
���������3A+B mC+2D
mC+2D
nʼ? 0.6mol��0.5mol? 0? 0
n��?0.3mol? 0.1mol? 0.1m? 0.2mol
nƽ?0.3mol? 0.4mol? 0.1m? 0.2mol
0.1m? =? 0.2mol? m=1B��ת����Ϊ20% ,A��ƽ����Ӧ����Ϊ0.15mol��L-1��min-1? ,B ��ȷ��C����ƽ��ʱ��Ӧ����������ʵ���Ϊ1.1,mol,D����
�����Ѷȣ���
4��ѡ���� ���ڿ��淴Ӧ2AB3(g)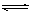 A2(g) +3B2(g)������Ӧ���ȣ�����ͼ����ȷ����
A2(g) +3B2(g)������Ӧ���ȣ�����ͼ����ȷ����
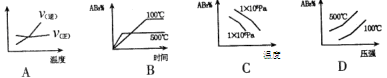
�ο��𰸣�B
����������ӷ���ʽ�ɿ������ÿ��淴Ӧ������Ӧ��һ�����������������ȷ�Ӧ��������������ԭ��������ѹǿ����ѧƽ�����淴Ӧ�����ƶ��������¶ȣ���ѧƽ��������Ӧ�����ƶ��������¶ȣ���ѧ��Ӧ���ʼӿ죬�ﵽ��ѧƽ����Ҫ��ʱ���Խ�١�Aͼ���淴Ӧ��ƽ��������¶ȣ�����V(��)��v(��)����ѧƽ�����淴Ӧ�����ƶ���������Ŀ������Ӧ������Υ��������B�����¶ȣ���ѧƽ��������Ӧ�����ƶ�����Ӧ���ת����Խ�ߣ��ﵽƽ��ʱ���ĺ�����Խ�٣���ȷC����ѹǿ����ѧƽ�����淴Ӧ�����ƶ��� AB3Ӧ��Խ�࣬��ѡ����ѹǿ��ʱ��Ӧ�����ƽ��ʱ���������٣�����Dͼ �����¶ȣ�ƽ��ʱ��Ӧ��ĺ�����Խ�ߣ����뻯ѧƽ��������ʱ������Ӧ�����ƶ���Υ��������
�����Ѷȣ�һ��
5��ѡ���� ��һ���¶��µĶ��ݵ������У���������Щ���������ٷ����仯ʱ��������ӦA��g��+2B��g���TC��g��+D��g���Ѵﵽƽ��״̬���ǣ�������
�ٻ�������ѹǿ?�ڻ��������ܶ�?��B�����ʵ���Ũ��? �ܻ�����������ʵ���? �ݻ�������ƽ����Է�������?
�����ʹ�ϵ��v��C����v��D���ı�ֵ? �������������? ���������������
A���٢ڢۢܢݢޢߢ�
B���٢ۢܢ�
C���٢ڢۢܢݢ�
D���٢ۢܢݢ�
�ο��𰸣��ٸ÷�ӦΪ��Ӧǰ����������ʵ�����С�ķ�Ӧ������������䣬�淴Ӧ����ѹǿ���ͣ���ѹǿ���ٱ仯��˵������ƽ�⣬�ʢ���ȷ��
�ڷ�Ӧ����ﶼ�����壬���������䣬����������䣬�ܶ���ʼ���ն����䣬����˵������ƽ��״̬���ʢڴ���
���淴Ӧ����B��Ũ�ȼ�С����B�����ʵ���Ũ�Ȳ��ٱ仯��˵������ƽ�⣬�ʢ���ȷ��
�ܸ÷�ӦΪ��Ӧǰ����������ʵ�����С�ķ�Ӧ���淴Ӧ���л�����������ʵ�����С��������������ʵ������ٱ仯��˵������ƽ�⣬�ʢ���ȷ��
�ݷ�Ӧ����ﶼ�����壬���������䣬�淴Ӧ���л�����������ʵ�����С�������淴Ӧ���л�������ƽ����Է�������������������ƽ����Է����������ٱ仯��˵������ƽ�⣬�ʢ���ȷ��
��v��C����v��D�������ʹ�ϵ��ʼ���ն���1��1������˵������ƽ�⣬�ʢ���
�߷�Ӧ����ﶼ�����壬��������������������仯������˵������ƽ�⣬�ʢߴ���
��������������䣬���������������䣬����˵������ƽ�⣬�ʢ����
�ʢ٢ۢܢ���ȷ��
��ѡ��B��
���������
�����Ѷȣ���