1������� X��Y��Z��W��Ԫ�����ڱ�ǰ�������еij���Ԫ�أ��������Ϣ���±���
Ԫ��
| �����Ϣ
|
X
| X��ij���⻯����ʹʪ��ĺ�ɫʯ����ֽ����
|
Y
| ���������õİ뵼����ϣ��㷺Ӧ���ڹ����Ϣ����
|
Z
| Z��һ�ֺ���������Ϊ27��������Ϊ14
|
W
| ����������Ӧ��ˮ������һ�ֲ�����ˮ����ɫ����
|
��1��Zλ��Ԫ�����ڱ��� ���ڵ� �壬W��̬ԭ�ӵĺ�������Ų�ʽΪ
��2��X�ĵ�һ�����ܱ�Y�� �����С������X�ĵ��ʷ����ЦҼ��ͦм�����Ŀ��Ϊ ��Y���������� ���塣
��3��X���⻯�X2H4�����Ʊ�����֮һ�ǽ�NaC1O��Һ��XH3��Ӧ�Ƶã���д���÷�Ӧ�Ļ�ѧ����ʽ ��
��4����֪�������ݣ�
4W(s)+O2(g)��2W2O(s) ��H��һ337.2kJ��mol��1
2W(s)+O2(g)��2WO(s) ��H��һ314.6kJ��mol��1
��W2O��O2��Ӧ����WO���Ȼ�ѧ����ʽ�� ��
2������� ����ѧ֪ʶϵͳ���������ڶԻ�ѧ����Ľ�һ����ʶ�����⡣
����1����ѧ��Ӧ����ײ���ۣ���Ӧ����Ӽ�����ײ�Ƿ�Ӧ���еı�Ҫ��������������ÿ����ײ��������Ӧ��ֻ��������ײ���ܷ�����ѧ��Ӧ����������ѧ��Ӧ����ײ��֮Ϊ��Ч��ײ��
����2����ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ������ͨ������ײ������ɵģ������ڷ�Ӧ�ﵽ������Ĺ����о���һ���������Ĺ���̬��
����3����ѧ��Ӧ�������仯(��H)�뷴Ӧ���������ļ����йء�������ѧ��̬��298K��1.01��105Pa���£����ȶ��ĵ��ʷ�����Ӧ����1mol������ķ�Ӧ�Ƚиû�����������ȣ���H����
�����������ϻش��������⣺
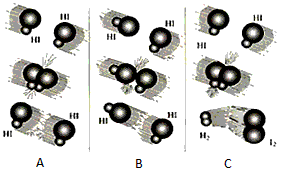
��1����ͼ��HI�ֽⷴӦ��HI����֮��ļ�����ײʾ��ͼ������������Ч��ײ���� __________________��ѡ�A������B����C������
��2����ͼ��1molNO2��CO��Ӧ����CO2��NO�����������仯ʾ��ͼ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ�� ___________________________________________��
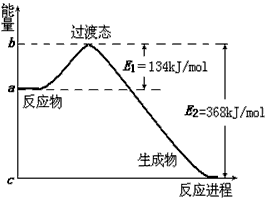
��3�� �±��Dz��ֻ�ѧ���ļ�������
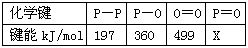
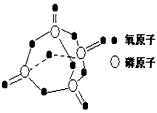
��֪����ȼ����Ϊ2378.0 kJ/mol��������ȫȼ�յIJ���ṹ(P4O10)���ϣ��ң�ͼ��ʾ�����ϱ���X��
_______________________________��
��4����ͼΪ����Ԫ�ص��⻯��a��b��c��d������������ʾ��ͼ��
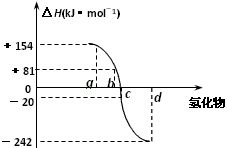
������ɣ��ǽ���Ԫ�ص��⻯����ȶ������⻯��������ȣ���H��֮��Ĺ�ϵ��_____________________________________��
3��ѡ����
�����Ȼ�ѧ����ʽ����101kPaʱ����S��s��+O2��g���TSO2��g����H=-297.23kJ/mol����������˵���в���ȷ����
�� ? ��
A��S��ȼ����Ϊ297.23?kJ/mol
B���γ�1?mol?SO2�Ļ�ѧ�����ͷŵ����������ڶ���1?mol?S��s����1?mol?O2��g���Ļ�ѧ�������յ�������
C��S��g��+O2��g���TSO2��g���ų�������С��297.23?kJ
D��S��g��+O2��g���TSO2��g���ų�����������297.23?kJ
4��ѡ���� ʵ���ã�101 kPaʱ��1 mol H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ��������1 mol CH4��ȫȼ������Һ̬ˮ��CO2���ų�890.3 kJ�������������Ȼ�ѧ����ʽ����д��ȷ����
��CH4(g)��2O2(g)=CO2(g)��2H2O(l) ��H����890.3 kJ��mol��1
��CH4(g)��2O2(g)=CO2(g)��2H2O(l) ��H����890.3 kJ��mol��1
��CH4(g)��2O2(g)=CO2(g)��2H2O(g) ��H����890.3 kJ��mol��1
��2H2(g)��O2(g)=2H2O(l) ��H����571.6 kJ��mol��1
A������
B�����Тڢ�
C�����Тڢۢ�
D��ȫ������Ҫ��