1、选择题 在一固定容积的密闭容器中,充入3mol?A?和1mol?B,发生反应:3A(g)+B(g)?xC(g),达平衡后,C的浓度为a?mol/L,若维持容器体积和温度不变,以0.6mol?A、0.2mol?B和1.6mol?C为起始物质,达到平衡后,C的浓度也为a?mol/L,则x的值为( )
A.1
B.2
C.3
D.4
参考答案:恒温恒容下,开始充入3molA和1molB与开始充入0.6molA、0.2molB和1.6molC达到平衡后,C的浓度都为amol/L,说明为完全等效平衡,按化学计量数转化到左边,满足n(A)=3mol、n(B)=1mol,故0.6mol+3x×1.6mol=3mol,0.2mol+1x×1.6mol=1,解得x=2,
故选B.
本题解析:
本题难度:简单
2、选择题 哈伯因发明了用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3 molH2,在高温高压催化剂共存的条件下使该反应发生。达到平衡时,下列说法正确的是


A.N2完全转化为NH3
B.N2、H2和NH3的物质的量浓度一定相等

C.N2、H2和NH3的物质的量浓度不再变化
D.正反应和逆反应速率都为零
参考答案:C
本题解析:A、可逆反应反应物不能完全反应,故A错误;B、反应平衡时各物质的浓度是否相等取决于起始时各物质的量的关系和转化的程度,N2、H2按1:3混合,化学计量数为1:3,所以转化率相等,平衡时,N2、H2的物质的量浓度一定为1:3,故B错误;C、随反应进行,N2、H2和NH3的物质的量浓度发生变化,N2、H2和NH3的物质的量浓度不再变化,说明到达平衡状态,故C正确;D、可逆反应时动态平衡,达到化学平衡时,正反应和逆反应的速率,但不为零,故D错误.故选:C
本题难度:简单
3、选择题 反应H2(g)+ I2(g) 
 ?2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是(? )
?2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是(? )
①单位时间内断裂n mol H-H键的同时形成2n mol H-I键 ②单位时间内生成n molI2的同时生成2n molHI?
A.②④⑤⑥
B.②③④⑤
C.①③④⑤
D.全部
参考答案:B
本题解析:达到化学平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于化学计量数之比(不同物质),各物质的浓度、质量、物质的量、百分含量不变。①单位时间内断裂n mol H-H键的同时形成2n mol H-I键,都描述的正反应方向的变化,错误;②单位时间内生成n molI2的同时生成2n molHI,说明反应v正=v逆,达到平衡状态,正确;③2v正(H2)=v逆(HI),正确;④HI分子数不再改变,即其浓度不再改变,正确;⑤混合气体颜色不再改变,即碘单质的浓度不再改变,正确;⑥该化学反应是气体物质的量不变的反应,故混合气体压强不再改变不能用来判断是否平衡,故错误。
本题难度:一般
4、填空题 高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂。
(1)FeO42-与水反应的方程式为:4FeO42- + 10H2O  ?4Fe(OH)3 + 8OH-+ 3O2,
?4Fe(OH)3 + 8OH-+ 3O2,
K2FeO4在处理水的过程中所起的作用是?和?。

(2)将适量K2FeO4配制成c(FeO42-) =1.0×10-3 mol・L-1(1.0mmol・L-1)的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图Ⅰ。题(1)中的反应为FeO42-变化的主反应,该反应的△H?0。
(3)FeO42-在水溶液中的存在形态如图Ⅱ所示。下列说法正确的是?(填字母)。
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.改变溶液的pH,当溶液由pH=10降至pH=4的过程中,HFeO4-的分布分数先增大后减小
C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为:H2FeO4+OH-=HFeO4-+H2O
D.pH约为2.5 时,溶液中H3FeO4+和HFeO4-比例相当
(4)HFeO4- H++FeO42-的电离平衡常数表达式为K=___________________,其数值接近?(填字母)。
H++FeO42-的电离平衡常数表达式为K=___________________,其数值接近?(填字母)。
A.10-2.5?B.10-6?C.10-7?D.10-10
(5)25℃时,CaFeO4的Ksp = 4.536×10-9,若要使100mL,1.0×10-3 mol・L-1的K2FeO4溶液中的c(FeO42- )完全沉淀,理论上至少要加入的Ca(OH)2的物质的量为?mol,
完全沉淀后溶液中残留的c(FeO42- )为______________。
参考答案:(1)杀菌消毒,吸附杂质(2)>(3)BD(4)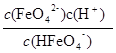 ?C(5)4.536×10-5,1×10-5mol/L
?C(5)4.536×10-5,1×10-5mol/L
本题解析:(1)FeO42-具有强氧化性,能消毒杀菌;FeO42-与水生成的Fe(OH)3胶体能吸附水中的悬浮物,使水体净化。(2)由图I可以看出,温度越高,溶液中c(FeO42-)越小,说明升高温度,平衡向右移动,所以正反应是吸热反应。(3)由图可知当pH小于1.5时,溶液中只有H3FeO4+和H2FeO4,A错误;pH由10降至4时,HFeO4-的分布分数先增大后减小,B正确;向pH=8的该溶液中加KOH溶液,pH增大,离子方程式为HFeO4-+OH-=FeO42-+H2O,C错误;pH约为2.5 时, H3FeO4+和HFeO4-分布分数相等,D正确。(4)HFeO4- H++FeO42-的电离平衡常数K=
H++FeO42-的电离平衡常数K=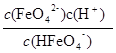 ,当pH接近7时,c(FeO42-)=c(HFeO4-),K≈10-7。(5)要形成CaFeO4沉淀,必须c(Ca2+)・c(FeO42-)>Ksp(CaFeO4)。
,当pH接近7时,c(FeO42-)=c(HFeO4-),K≈10-7。(5)要形成CaFeO4沉淀,必须c(Ca2+)・c(FeO42-)>Ksp(CaFeO4)。
点评:勒沙特列原理适用于所有平衡体系;两种溶液混合,形成沉淀的条件是Q>Ksp。
本题难度:困难
5、填空题 (5分)可逆反应3A(g) 3B(?)+C(?)? △H>0达到化学平衡后,
3B(?)+C(?)? △H>0达到化学平衡后,
(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
a.若B、C都是气体,气体的平均相对分子质量①?;
b.若B、C都不是气体,气体的平均相对分子质量?② ;
c.若B是气体,C不是气体,气体的平均相对分子质量③ ;
(2)如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是④?态,C是⑤?态。
参考答案:①变小?②不变?③变小?④固态或液态?⑤气态(各1分共5分)
本题解析:可逆反应3A(g) 3B(?)+C(?)? △H>0?,
3B(?)+C(?)? △H>0?,
气体的平均相对分子质量=m气体总/n气体总
a.若B、C都是气体,反应前后,气体质量守,而且该反应是气体体积增大的反应,升高温度 ,平衡向正向移动,即向体积增大的方向移动, 所以气体的平均相对分子质量变小。
b.若B、C都不是气体,只有反应物是气体所以反应前后,气体的平均相对分子质量不变。
若B是气体,C不是气体,反应前后,气体质量减少,而气体体积反应前后不变,所以气体的平均相对分子质量变小;如果平衡后保持温度不变,将容器体积增加一倍,如果平衡不再移动,新平衡时A的浓度是原来的50%,但是新平衡时A的浓度是原来的60%,说明平衡向逆反应方向移动,即,减小压强,平衡向体积增大的方向移动,该方向是逆向,所以反应前的气体体积数大于反应后的气体体积数,则B是固态或液态? C是气态。
点评:解答此类试题要求学生对反应前后体积变化的反应,气体的平均相对分子质量是不是变化,要看气体的平均相对分子质量=m气体总/n气体总中气体总质量和气体总的物质的量是不是变化来分析。
本题难度:一般