1、简答题 50mL?1.0mol?L-1盐酸与50mL?1.1mol?L-1氢氧化钠溶液在如图装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:
(1)大小烧杯间填满碎泡沫塑料的作用:______.
(2)______(填“能”或“不能”)将环形玻璃搅拌棒改为环形金属(如铜)棒;原因是:______.
(3)实验用50mL?1.1mol?L-1氢氧化钠溶液的原因是:______.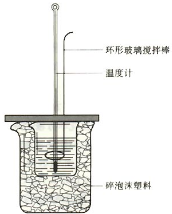
参考答案:(1)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是:减少实验过程中的热量损失,故答案为:减少实验过程中的热量损失;
(2)不能将环形玻璃搅拌棒改为环形金属(如铜)棒,因为环形金属棒是热的良导体,故答案为:不能;因为环形金属棒是热的良导体;
(3)因盐酸易挥发,会导致热量散失,则用过量的氢氧化钠保证盐酸反应完全,以盐酸的量为准进行准确计算,故答案为:要保证盐酸反应完全,以盐酸的量为准进行准确计算.
本题解析:
本题难度:一般
2、选择题 下列说法正确的是( )
A.活化分子之间发生碰撞就是有效碰撞,一定生成新的物质
B.1mol硫酸与1mol氢氧化钡完全反应所放出的热量在数值上等于中和热
C.1molC与氧气反应生成1molCO所放出的热量,就是C的燃烧热
D.对于反应:2SO2+O2?2SO3△H<0,升高温度时,正、逆反应速度都加快
参考答案:D
本题解析:
本题难度:一般
3、实验题 中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
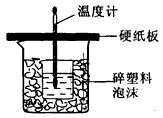
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是_________________________________。
(2) 大烧杯上如不盖硬纸板,则求得的中和热数值_________(填“偏大”.“偏小’.“无影响”)
(3) 实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),理由是____________________________________________________;所求中和热的数值会________(填“相等”或 “不相等”),理由是________________________________________________________。
参考答案:
(1)环形玻璃搅拌棒;保温、隔热,减少实验过程中的热最损失
(2)偏小
(3)不相等; 因为酸、碱发生中和反应放出的热量与酸、碱的用量有关; 相等; 中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量,它与酸、碱的用量无关
本题解析:
本题难度:一般
4、选择题 在中和热测定的实验中不需要用到的仪器是( )
A.量筒
B.温度计
C.环形玻璃搅拌棒
D.天平
参考答案:D
本题解析:
本题难度:简单
5、选择题 己知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液,H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol
下列结论正确的是( )
A.碳的燃烧热大于110.5kJ/mol
B.①的反应热为221kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
参考答案:A
本题解析:
本题难度:一般