|
|
|
高中化学知识点归纳《盐类水解的原理》试题预测(2019年最新版)(十)
2019-07-03 23:20:20
【 大 中 小】
|
1、选择题 某温度下,Kw=10―13,已知该温度下某浓度Na2CO3溶液的pH=10,则该溶液中由水电离的c(OH―)是
A.1×10―10 mol/L
B.1×10―3 mol/L
C.1×10―4 mol/L
D.1×10―7 mol/L
|
参考答案:B
本题解析:
试题解析:pH=10,则氢离子浓度=10―10,c(OH-)=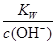 = = =10―3。 =10―3。
考点:溶液PH的计算
本题难度:一般
2、填空题 雾霾含有大量的污染物SO2、NO。工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

(1)装置Ⅰ中的主要离子方程式为 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如图所示。
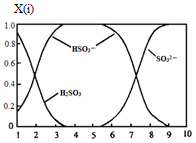
①若是0.1molNaOH反应后的溶液,测得溶液的pH=8时,溶液中个离子由大到小的顺序是 。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
(3)写出装置Ⅱ中,酸性条件下的离子方程式 。
(4)装置Ⅲ还可以使Ce4+再生,其原理如下图所示。
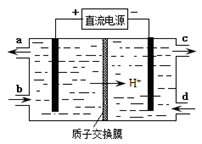
①生成Ce4+从电解槽的 (填字母序号)口流出。
②写出与阴极的反应式 。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g・L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)
参考答案:(每空2分)
(1)SO2 + OH-="==" HSO3-
(2)①c(Na+>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
②HSO3- 在溶液中存在电离平衡:HSO3- SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。 SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。
(3)NO+2H2O+3Ce4+===3Ce3++NO3-+4H+、NO+H2O+Ce4+===Ce3++NO2-+2H+
(4)①a ②2HSO3-+4H++ 4e-="==" S2O32-+3H2O
(5)243a(242a、244a、5600a /23都给分)
本题解析:(1)装置Ⅰ中的将SO2变成了HSO3-,离子方程式是SO2 + OH-="==" HSO3-。
(2)①若是0.1molNaOH反应后的溶液,测得溶液的pH=8时,图像中的c(SO32-)>c(HSO3-),而c(OH-)=10-6mol/L,远小于c(OH-),故溶液中离子浓度为:c(Na+>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)。②HSO3- 在溶液中存在电离平衡:HSO3- SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。 SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。
(3)在酸性条件下装置Ⅱ中,Ce4+将NO氧化为NO3-或NO2-,本身还原为Ce3+,有两个反应,即NO+2H2O+3Ce4+===3Ce3++NO3-+4H+、NO+H2O+Ce4+===Ce3++NO2-+2H+。
(4)装置Ⅲ使Ce3+→Ce4+,反应过程失去电子,在阳极发生,接电源正极,故生成Ce4+从电解槽的a口出来;阴极HSO3-得到电子生成S2O32,即2HSO3-+4H++ 4e-="==" S2O32-+3H2O。
(5)装置Ⅳ中的与O2和NO2-参加的反应:2NH3+2H++O2+2NO2-===2NH4NO3,n(O2)=n(NO2-)= ×1000L×a g・L-1/46g・mol-1,V(O2)=22.4L・mol-1 n(O2)= 243a。
考点:离子方程、电极反应式的书写及简单化学计算。
本题难度:困难
3、选择题 在25ºC时,某氯化铵溶液的pH=4,下列说法中不正确的是:
A.溶液中c(H+)>c(OH-),且Kw=c(H+).c(OH-)=1×10-14mol2/L2
B.由水电离出来的H+浓度为1×10-4mol/L-1
C.溶液中c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.此溶液中由水电离出来的c(H+)=c(OH-)
|
参考答案:A
本题解析:A、该溶液水解呈酸性,
B、盐类水解促进水的电离,正确;
C、铵根水解生成氢离子和一水合氨;正确
D、任何溶液中水电离的氢离子等于氢氧根离子。正确
本题难度:简单
4、选择题 下面提到的问题中,与盐的水解无关的是
A.明矾和FeCl3可作净水剂
B.为保存FeCl3溶液,要在溶液中加少量盐酸
C.用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
D.氢氟酸用塑料试剂瓶保存而不用玻璃试剂瓶保存
参考答案:D
本题解析:A.明矾和FeCl3 可作净水剂依据铝离子、铁离子水解生成胶体具有较大的表面积,具有吸附悬浮杂质的作用;有关;B.加入盐酸抑制铁离子的水解,有关;C.碳酸氢根离子和铝离子发生双水解生成二氧化碳和氢氧化铝沉淀,有关;D.氢氟酸和玻璃反应,所以氢氟酸用塑料试剂瓶保存而不用玻璃试剂瓶保存,无关,选D.
考点:考查盐类水解的应用。
本题难度:一般
5、选择题 某一密闭绝热容器中盛有饱和Ca(OH)2溶液,当加入少量CaO粉末,下列说法正确的是
①有晶体析出 ②c[Ca(OH)2]增大 ③pH不变
④c(H+)・c(OH)-的积不变⑤c(H+)一定增大
A.①
B.①⑤
C.①②④
D.①③
参考答案:B
本题解析:氧化钙能和水反应生成氢氧化钙,同时放热。由于氢氧化钙是饱和溶液,且氢氧化钙的溶解度随温度的升高而降低,所以溶液中会析出晶体。溶解度降低,浓度减小,因此碱性降低,所以氢离子浓度增大答案选B。
本题难度:一般