1������� ����10�֣���ѧѧ���е�ƽ��������Ҫ���ݰ�������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ������֣��Ҿ�������������ԭ����
��1���ڹ̶��ݻ����ܱ������У���ӦA(g)+2B(g) 4C(g),
4C(g),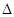 H ��0�ﵽƽ��ʱ���ı��������´ﵽƽ�����ϵ��A��ת���������е���? __
H ��0�ﵽƽ��ʱ���ı��������´ﵽƽ�����ϵ��A��ת���������е���? __
A������B�����ʵ���? B����ѹ? C������? D��ʹ�ô���
��2��ij��Һ���������ȵ�NaOH��Һ�ʹ����϶��ɣ���ǡ�ó����ԣ�����ǰc(NaOH) ____c(CH3COOH)����Ϻ���Һ��c(CH3COO-)____c(Na+)
��3�������£�ȡpH=2������ʹ�����Һ��100mL�������зֱ����������Zn��(������Zn���Է�Ӧ���ʵ�Ӱ��)����Ӧ����������Һ��pH�仯����ͼ��ʾ��

��ͼ�б�ʾ������Һ��pH�仯���ߵ���?����A��B�����������м����Zn����Ϊm1��������Һ�м����Zn����Ϊm2����m1?m2��ѡ��p=�p����
�ο��𰸣���1��AC��ÿ��1�֣�?��2���� ��=?��3��B�� ��
�����������1����Ӧ�������������ȷ��ȿ��淴Ӧ������Ҫ����A��ת���ʣ�ƽ��Ӧ��������Ӧ�����ƶ�������ѡ��AC�����ԡ���ѹƽ�����淴Ӧ�����ƶ����������ܸı�ƽ��״̬��������ȷ�Ĵ���AC��
��2����ǡ�÷�Ӧ���������������ˮ���Լ��ԣ����Ҫ�����ԣ�����һ���ǹ����ġ����������Ƶ�Ũ��С�ڴ���ġ�
��3��������������ʣ����ڵ���ƽ�⡣�ڷ�Ӧ�����л��������������ӣ����Դ����������ӵ�Ũ�ȱ仯�̶�С�����ᡣ���Ҫʹ��Ӧ���pH��ȣ��������Ҫ��ʱ��Ͷ࣬��B��ʾ����ġ����������ĵ������Ӷ࣬����Ӧ��п���ĵ�Ҳ�Ͷࡣ
�����Ѷȣ�һ��
2��ѡ���� ���ڻ�ѧƽ�ⳣ��������˵������ȷ����(����)?
A����ѧƽ�ⳣ�����淴Ӧ����������Ũ�ȵĸı���ı�?
B����ѧƽ�ⳣ�����¶ȵĸı���ı�?
C������һ���¶��µ�ͬһ����Ӧ��������Ӧ���淴Ӧ�Ļ�ѧƽ�ⳣ���ij˻�����1?
D���¶�Խ�ߣ�KֵԽ��
�ο��𰸣�D
�����������ѧƽ�ⳣ��K=������Ũ���ݵĻ�/��Ӧ��Ũ���ݵĻ�, ��ѧƽ�ⳣ��ֻ���¶��йأ������ʵ�Ũ���أ���A��B��ȷ
���ݻ�ѧƽ�ⳣ���ļ���ʽ����֪������һ���¶��µ�ͬһ����Ӧ��������Ӧ���淴Ӧ�Ļ�ѧƽ�ⳣ���ij˻�����1����C��ȷ��
D����Ȼ��ѧƽ�ⳣ��ֻ���¶��йأ��������ȷ�Ӧ���¶�Խ�ߣ�ƽ��������Ӧ�����ƶ���,KԽ���Ƿ��ȷ�Ӧ���¶�Խ�ߣ�ƽ�����淴Ӧ�����ƶ���KԽС���ʴ�
���������⿼���˻�ѧƽ�ⳣ���ĺ��壬�ѶȲ���ע�⻯ѧƽ�ⳣ��ֻ���¶��йأ����ǽ���Ĺؼ���
�����Ѷȣ�һ��
3��ѡ���� �йػ�ѧƽ�ⳣ��(K)��˵���в���ȷ���ǣ�?��
A����ֵԽ������Ӧ���еij̶�Խ��
B��һ���˵,K��105ʱ���÷�Ӧ���еþͻ�����ȫ��
C��ѹǿԽ��KֵԽ��
D��K�뷴Ӧ����������Ũ�ȱ仯��
�ο��𰸣�C
��������� ��ֵԽ������Ӧ���еij̶�Խ��A��ȷ��һ���˵,K��105ʱ���÷�Ӧ���еþͻ�����ȫ�ˣ���B��ȷ��������A(g)+B(g)  C(g)+D(g)�ķ�Ӧ��ѹǿ����û��Ӱ�죬��ѹǿԽ��Kֵ��һ��Խ��C����Ϊ�������ȷ�𰸣�K�뷴Ӧ����������Ũ�ȱ仯�أ�����һ�������ķ�Ӧ��K��ֵֻ���¶��йأ���D��ȷ��
C(g)+D(g)�ķ�Ӧ��ѹǿ����û��Ӱ�죬��ѹǿԽ��Kֵ��һ��Խ��C����Ϊ�������ȷ�𰸣�K�뷴Ӧ����������Ũ�ȱ仯�أ�����һ�������ķ�Ӧ��K��ֵֻ���¶��йأ���D��ȷ��
���������⿼���˻�ѧƽ�ⳣ�����ÿ����Ǹ߿�������ص���Ѷȣ�����Ҫ���յ���ƽ�ⳣ��ֻ���¶��йأ���ֵԽ������Ӧ���еij̶�Խ�� �������Ѷ����С�
�����Ѷȣ�һ��
4��ѡ���� ������, ��ӦaX(g)? ?bY(g) +cZ(g)�ﵽƽ���, ���������ѹ����ԭ����һ���Ҵﵽ��ƽ��ʱ, X�����ʵ���Ũ����0.1mol/L����0.19mol/L, �����ж���ȷ����:
?bY(g) +cZ(g)�ﵽƽ���, ���������ѹ����ԭ����һ���Ҵﵽ��ƽ��ʱ, X�����ʵ���Ũ����0.1mol/L����0.19mol/L, �����ж���ȷ����:
A��a��b+c
B��a��b+c
C��a��b+c
D��a��b="c"
�ο��𰸣�A
������������������ѹ����ԭ����һ��˲�䣬X��Ũ�ȱ�Ϊ0.2mol/L��������ƽ��ʱŨ����0.19mol/L����˵��������ѹǿƽ��������Ӧ�����ƶ���������Ӧ�������С�ģ���ѡA�������͡�ѡ����
�����Ѷȣ�һ��
5��ѡ���� ������,��������ЧӦ����Դ��ȱ������,����CO2��̼����Ӧ�õ��о��ܵ����ǵ����ӡ�ij�о�С�����÷�Ӧ:CO(g)+H2O(g) H2(g)+CO2(g) ��H="-41.2" kJ/mol�Ʊ�CO2��H2�Ļ������,����һ���о�CO2��H2�Բ�ͬ������Ȼ��ʱ�ں��������µķ�Ӧ����Ӧ�á�
H2(g)+CO2(g) ��H="-41.2" kJ/mol�Ʊ�CO2��H2�Ļ������,����һ���о�CO2��H2�Բ�ͬ������Ȼ��ʱ�ں��������µķ�Ӧ����Ӧ�á�
(1)��֪:850 ��ʱ��һ���Ϊ10 L�ĺ����ܱ�������,ͨ��һ������CO��H2O,CO��H2OŨ�ȱ仯��ͼ��ʾ:
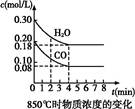
����˵����ȷ���ǣ�? ��?
A���ﵽƽ��ʱ,���������ʵ�����0.12 mol
B���ﵽƽ��ʱ,��Ӧ��ϵ���ջ�ų�49.44 kJ����
C����4 minʱ,��������ƽ����Է����������ٱ仯
D����6 minʱ,�������¶�,��Ӧƽ�ⳣ�����С
�ο��𰸣�BCD
������������������
�����Ѷȣ�һ��