1、选择题 下列分子中心原子是sp2杂化的是?
[? ]
A.PBr3?
B.CH4?
C.BF3?
D.H2O
2、填空题 分子式为Pt(NH3)2Cl2的配位化合物有顺铂和反铀两种同分异构体,顺铂的结构式为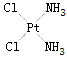
具有抗癌作用;反铂的结构式为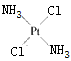 无抗癌作用
无抗癌作用
(1)C、N、O二种元素的电负性由大到小的顺序是_______________;Ni元素与Pt元素位于同一族,写出Ni元素基态原子的电子排布式_______________
(2)顺铂和反铂的物理性质有很大差异,其中只有一种易溶于水,请你通过所学知识判断哪一种易溶于水,并说明理由:________________。
(3)金属铂的原子堆积方式为面心立方最密堆积,一个金属铂的晶胞中含有_________个铂原子
(4)NH3还能与很多化合物通过配位键发生相互作用。例如:科学家潜心研究的一种可作储氢材料的化合物X是NH3与第二周期另一种元素的氢化物相互作用的产物,X是乙烷的等电子体;加热化合物X会缓慢释放H2,并转变为化合物Y,Y是乙烯的等电子体①化合物X的结构式为______________。(必须标明配位键)②化合物X、Y分子中,N元素分别发生了____________ 杂化。
3、填空题 已知a、b、x、y、z五种元素的原子序数依次增大,其中a原子的半径是所有原子中半径最小的,b原子中的电子有6种不同的运动状态,y原子的L层有2对成对电子,z元素的电负性是前四周期中最小的。
(1)x、y两种元素的第一电离能的大小为x________y(填“>”、“<”或“=”),用原子结构的知识解释原因________________________;
(2)固体物质M的化学式为xa5?,它的所有原子最外层都符合相应的稀有气体原子的最外电子层结构。则该化合物中a元素的化合价为_______和______;该化合物中x原子的杂化方式为__________;
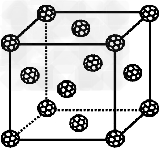
(3)如果把晶胞顶点与最近三个面心所围成的空隙叫做四面体空隙,z原子可作为容体掺入C60晶体的空隙中,形成具有良好的超导性的掺杂C60化合物。现把C60?抽象成质点,该晶体的晶胞结构如图所示,若每个四面体空隙填入一个z元素的原子,则?z元素全部填满C60晶体的四面体空隙后,所形成的掺杂C60化合物的化学式为_____________。
4、填空题 硼的单质和化合物在工业上有重要的应用。
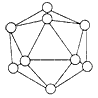
(1)晶体硼的基本结构单元都是由硼原子组成的正二十面体,其中含有20个等边三角形的面和一定数目的顶角,每个顶角各有一个硼原子。如图所示,则针对晶体硼的基本结构单元回答下列问题:
①B-B键间键角为_________;
②其中硼原子数有________个;B-B键有________根。
(2)B2O3与C3O2互为等电子体,试写出C3O2的结构式___________。
(3)硼酸[B(OH)3]是一种较弱的一元酸,眼科医院常用作消毒剂,在实验中不小心被碱溶液灼伤后清洗伤口后可涂上少量的硼酸,写出硼酸的电离方程式____________。在硼酸分 子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是
_______。
A.sp,范德华力 B.sp2,范德华力 C.sp2,氢键 D.sp3,氢键
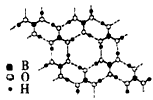
(4)在30℃以下,将过氧化氢加到硼酸和氢氧化钠的混合溶液中,析出一种无色晶体X。组成分析证实,该晶体的质量组成为Na 14. 72%,B 7.03%, H 5.12 %,则X的化学式为________。
5、填空题 铜(Cu)是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答下列问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为__________________;
(2)CuSO4粉末常用来检验一些有机物的微量水分,其原因是__________________;
(3)SO42-的立体构型是__________,其中S原子的杂化轨道类型是___________;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为___________;一种铜金合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心、Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为________;该晶体中,原子之间的作用力是__________;
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构相似,该晶体储氢后的化学式应为___________。