1��ʵ���� ��ѧ��Ӧ���ʵı仯�ͻ�ѧƽ���ƶ��Ĺ��ɶ�����ͨ��ʵ��ó����ۣ���������ԭ��Ҳ����ʵ���ܽ�����ġ�
��1����ͭƬͶ�뵽ϡ�����У���ʼʱ�������ݵ����ʺ�������� Ӧ������������ѧ����֪ʶ��������Ӧ���������ԭ����________________ __________________��������һ��ʱ���Ӧ�����ּ�����������ʼ�����ԭ����_______________________________��
Ӧ������������ѧ����֪ʶ��������Ӧ���������ԭ����________________ __________________��������һ��ʱ���Ӧ�����ּ�����������ʼ�����ԭ����_______________________________��
��2����ͪ�͵���������Һ�з������з�Ӧ��CH3COCH3��I2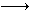 CH3COCH2I��H����I����25��ʱ���÷�Ӧ�����������о��鹫ʽ������
CH3COCH2I��H����I����25��ʱ���÷�Ӧ�����������о��鹫ʽ������
�ԣ�k?c��CH3COCH3��?c��H����[mol/��L?s��]
���ݸþ��鹫ʽ�����c��I2����c��CH3COCH3����c��H��������ʼŨ������Ϊ0��01 mol/L��0��1 mol/L��0��01 mol/L��������Ӧ���ʵı仯������_______________ ________________��
��3����һ֧�Թ����ȼ���30 mL 0��01 mol/L FeCl3��Һ���ٵμ�10 mL 0��01 mol/L KSCN��Һ��ҡ�ȡ����Ƶõ���Һƽ����װ��4֧�Թ��У�Ȼ��ֱ���룺��FeCl3���壻��KSCN���壻��KCl���壻��H2O���������Һ����ɫ�����������________������ţ���
��4����50 mL��ע����������40 mL NO2��N2O4�Ļ�����壬����һͬ������ע����������40 mL Br2��g�����Ա���ע�������������ɫ��ȫһ�¡�Ȼ��ע�����Ļ�����������20 mL��������ע�������������ɫ�仯��������___________________________���Ʋ�ƽ���ƶ���ͨ���۲�װ��NO2��N2O4�Ļ�������ע�������������ɫ��װ��Br2��g����ע�������������ɫ_______��
��5�����Ҫ�����ܷ�����������ͨ���ܱ������г����ĺ���ɫ������NO2��N2O4���������Br2��g��������____________________��
�ο��𰸣���1���÷�Ӧ�Ƿ��ȷ�Ӧ��1�֣������ŷ�Ӧ�Ľ��У������Ũ�ȼ�С��1�֣���
��2�������������С?��2�֣���
��3����?��2�֣���
��4��ǰ���ȱ�����dz������ԭ�������ֻ����?��2�֣���?dz?��2�֣���
��5��ͨ�����ȣ�����������Ҳ�ɣ�?��2�֣���
�����������
�����Ѷȣ�һ��
2��ѡ���� ����100mL1mol/L��������������Ƭ��Ӧ����ȡ���д�ʩ��ʹ��Ӧ���ʼӿ���H2�IJ���������ǣ��������¶ȣ��ڸ���100mL18mol/L����۸���100mL2mol/L��������������۴�����Ƭ���ݵ�������CuSO4��Һ��������
A���٢ۢ�
B���٢ܢ�
C���ڢۢ�
D���٢ڢ�
�ο��𰸣��������¶ȣ�ʹ��Ӧ���ʼӿ���H2�IJ������䣬����ȷ��
�ڸ���100mL18mol/L���ᣬ����������ԭ��Ӧ�������������ʴ���
�۸���100mL2mol/L���ᣬ����������ԭ��Ӧ�������������ʴ���
�����������۴�����Ƭ������Ӵ������ʹ��Ӧ���ʼӿ���H2�IJ������䣬����ȷ��
�ݵ�������CuSO4��Һ������ԭ��أ�ʹ��Ӧ���ʼӿ���H2�IJ������䣬����ȷ��
��ѡB��
���������
�����Ѷȣ�һ��
3������� ��400 �桢101 kPaʱ��NO2(g)��CO(g)==NO(g) + CO2(g)��Ӧ���̵������仯����ͼ��ʾ��
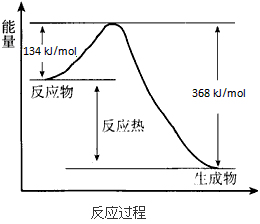
��1���÷�Ӧ��________������ȡ����ȡ�����Ӧ��
��2���÷�Ӧ���Ȼ�ѧ����ʽΪ________________��
��3���ı�������������ʹ�÷�Ӧ�ķ�Ӧ���ʸı䣬����ͨ�����ͻ�ܼӿ췴Ӧ���ʵ���_______��
a��Ũ�� b��ѹǿ c���¶� d������
�ο��𰸣���1������
��2��NO2(g)��CO(g) NO(g) + CO2(g) ��H=-234 kJ/mol
NO(g) + CO2(g) ��H=-234 kJ/mol
��3��d
���������
�����Ѷȣ�һ��
4��ѡ���� ������Fe����һ���������ᷴӦ��Ϊ�˼�����Ӧ���ʣ����ֲ�Ӱ�����������������Ӧ�������������е�
A��NaNO3��Һ
B��NaCl����
C��Na2SO4��Һ
D��CuSO4��ĩ
�ο��𰸣�C
���������
���������ݷ����ķ�ӦΪFe+2H+�TFe2++H2�������С�����ӵ�Ũ�ȶ����ı������ӵ����ʵ����������������Ӧ���ʣ����ֲ�Ӱ������������������Դ������
�⣺���ݷ����ķ�ӦΪFe+2H+�TFe2++H2�������С�����ӵ�Ũ�ȶ����ı������ӵ����ʵ����������������Ӧ���ʣ����ֲ�Ӱ�����������������
A������NaNO3��Һ��Fe����������ӡ������ӷ���������ԭ��Ӧ����NO������������������A����
B������NaCl���壬�Է�Ӧ��Ӱ�죬���������Ӧ���ʣ���B����
C������Na2SO4��Һ�������Ʋ����뷴Ӧ����Һ�������������ӵ�Ũ�ȼ�С���������ӵ����ʵ���û�б仯����Ӧ���ʼ��������ֲ�Ӱ�������������������C��ȷ��
D������CuSO4������Fe��Cu������ԭ��أ��ӿ췴Ӧ���ʣ���D����
��ѡC��
�����Ѷȣ�һ��
5��ѡ���� ������������H2C2O4���Ա�KMnO4��Һ������ʹKMnO4��Һ��ɫ������KMnO4��Һ��ɫʱ��ij��̿��ԱȽϷ�Ӧ���еĿ��������и���ʵ������Һ��ɫ����һ����
[? ]
����Ӧ�¶�/�桡KMnO4(V/mL c/mol/L)��H2C2O4(V/mL c/mol/L)��MnSO4(m/g)
A.����20������������4��0.1����������������2��0.1��������������0
B.����20������������4��0.1����������������2��0.1��������������0.1
C.����40������������4��0.1����������������2��0.1��������������0
D.����40������������4��0.1����������������2��0.1��������������0.1
�ο��𰸣�D
���������
�����Ѷȣ�һ��