1、填空题 反应A(g)+B(s)?C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率:
(1)升温______;?(2)增大压强______;?(3)增大容器容积______;
(4)加入A______;?(5)加入B______;?(6)加正催化剂______.
参考答案:(1)升高温度,化学反应速率加快,故答案为:加快;?
(2)增大压强,化学反应速率加快,故答案为:加快;?
(3)增大容器容积,反应体系中物质的浓度变小,或认为压强减小,反应速率减慢,故答案为:减慢;?
(4)加入A,反应物的浓度增大,所以反应速率加快,故答案为:加快;?
(5)反应体系中只有B为纯固体,则加入B,反应速率不变,故答案为:不变;?
(6)加正催化剂,反应速率加快,故答案为:加快.
本题解析:
本题难度:一般
2、选择题 下列说法正确的是( )
A.Fe和Mg与0.1 mol・L-1的盐酸反应,反应速率相同
B.0.1 mol・L-1的盐酸与0.1 mol・L-1H2SO4分别与大小、形状相同的大理石反应,反应速率相同
C.催化剂能降低分子活化时所需能量,使单位体积内活化分子百分数大大增加
D.100 mL 2 mol・L-1的盐酸与锌片反应,加入适量的NaCl溶液,反应速率不变
参考答案:C
本题解析:A项中化学反应速率由反应物本身性质决定,Fe、Mg性质不同,反应速率不同;B项中大理石实质上与H+反应,盐酸中c(H+)="0.1" mol・L-1,硫酸中c(H+)="0.2" mol・L-1,所以速率不相同;D项中加入NaCl溶液,因为反应实质是Zn+2H+ Zn2++H2↑,H+浓度减小,故速率减小。
Zn2++H2↑,H+浓度减小,故速率减小。
本题难度:一般
3、选择题 下列说法正确的是(? )
A.增大压强,活化分子数增加,化学反应速率一定增大
B.升高温度,活化分子百分数增加,化学反应速率一定增大
C.活化分子间所发生的碰撞就是有效碰撞
D.加入反应物,使活化分子百分数增加,化学反应速率增大
参考答案:B
本题解析:增大压强,只能使气体反应物浓度增大,且活化分子总数不变,只是单位体积内活化分子数增多。故A、D错,活化分子间的碰撞不一定都是有效碰撞,故C错。
本题难度:简单
4、选择题 实验室用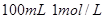 盐酸与锌粉反应,下列措施能使反应速率加快的是
盐酸与锌粉反应,下列措施能使反应速率加快的是
A.降低温度
B.改用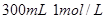 盐酸
盐酸
C.改用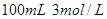 盐酸
盐酸
D.用等量锌粒代替锌粉
参考答案:C
本题解析:考查外界条件对反应速率的影响。在其他条件不变的时,增大反应物的浓度或升高温度或增大反应物的接触面积等均可以加快反应速率,所以选项C正确。
本题难度:一般
5、选择题 加入正催化剂使反应速率加快,下列叙述不正确的是( )
A.使反应体系的活化能降低
B.使反应体系的活化分子总数增多
C.使正反应速率增大,逆反应速率减小
D.使反应体系的活化分子百分数增大
参考答案:A、加入正催化剂使反应体系的活化能降低,进而使反应速率加快,故A正确;
B、正催化剂使反应体系的活化分子总数增多,故B正确;
C、催化剂能同等程度的改变正逆反应速率,加入正催化剂使正反应速率增大,逆反应速率也增大,故C错误;
D、催化剂可以使反应体系的活化分子百分数增加,故D正确.
故选C.
本题解析:
本题难度:一般