1������� ��2molSO2��1molO2��������ݻ�Ϊ2L���ܱ������У���800Kʱ���������·�Ӧ��2SO2��g��+O2��g��?2SO3��g����H��0������Ӧ�ӿ�ʼ���е�5minʱ����Ӧ�ﵽƽ��״̬����û�����������ʵ���Ϊ2.1mol����ش��������⣺
��1��800Kʱ���÷�Ӧ��ƽ�ⳣ��Ϊ______����0��5minʱ������SO2�ķ�Ӧ����Ϊ______��
��2������5minʱ�����¶ȣ���ijһʱ�����´ﵽƽ��״̬������ƽ������������������ʵ���______2.1mol�����������������=��������������ж����ɣ�______��
��3������ͬ�����£���������ڷֱ����xmolSO2��ymolO2��zmolSO3����Ӧ�ﵽƽ��ʱ�������ڻ�����������ʵ�����Ϊ2.1mol����x��y��z��������Ĺ�ϵ��______����һ���ú�x��z��ʽ�ӱ�ʾ��һ���ú�y��z��ʽ�ӱ�ʾ��
��4����ͬ�����£��������������У�����0.2mol?SO2��0.4mol?O2��4.0molSO3�������壬���жԸ÷�Ӧ״̬�������У���ȷ����______������ĸ��ţ���
A������ƽ��״̬?B������ƽ��״̬����Ӧ�������?C������ƽ��״̬����Ӧ������У�
�ο��𰸣���1����ƽ��ʱSO2��Ũ�ȱ仯��Ϊcmol/L����
? ?2SO2��g��+O2��g��?2SO3��g��
��ʼ��mol/L����1? 0.5? 0
�仯��mol/L����c? 0.5c? ?c
ƽ�⣨mol/L����1-c? ?0.5-0.5c? c
���ԣ�1-c��mol/L��2L+��0.5-0.5c��mol/L��2L+cmol/L��2L=2.1mol
��ã�c=0.9
��ƽ��ʱSO2��O2��SO3��Ũ�ȷֱ�Ϊ0.1mol/L��0.05mol/L��0.9mol/L��
��ƽ�ⳣ��k=c2(SO3)c2(SO2)?c(O2)=0��920��12��0.05=1620��
��v��SO2��=0.9mol/L5min=0.18?mol/��L?min����
�ʴ�Ϊ��1620��0.18?mol/��L?min����
��2������Ӧ��һ�����������ʵ�����С�ķ�Ӧ�����Ƿ��ȷ�Ӧ���������¶�ʱ��ƽ��������Ӧ�����ƶ�������ƽ��ʱ�����������ܵ����ʵ�����С��
�ʴ�Ϊ����������Ӧ��һ�����������ʵ�����С�ķ�Ӧ���ҷ��ȣ��������¶�ʱ��ƽ��������Ӧ�����ƶ���
��3�����º����£���Ӧǰ����������ʵ��������仯������ѧ������ת��Ϊ��ߣ�����n��SO2��=2mol��n��O2��=1mol���ɣ��ɷ���ʽ?2SO2��g��+O2��g��?2SO3��g����֪��zmolSO3��ȫת���ɵ�SO2Ϊzmol���ɵ�O2Ϊ0.5zmol��������x+z=2��y+0.5z=1��
�ʴ�Ϊ��x+z=2��y+0.5z=1��
��4������0.2mol?SO2��0.4mol?O2��4.0molSO3�������壬��ʱŨ����Qc=(4mol2L)2(0.2mol2L)2��0.4mol2L=2000��1620������ƽ��״̬����Ӧ������У���ѡC��
���������
�����Ѷȣ�һ��
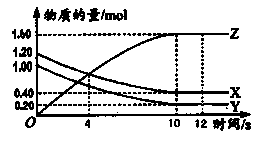
2��ѡ���� ij��Ӧ�У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯��ͼ��ʾ������˵����ȷ����
A����ӦΪ X + 2Z= Y
B����ӦΪ X + Y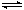 2Z
2Z
C��4 s ʱ����Ӧ�ﵽƽ��
D��12 s ʱ����Ӧ���ٽ���
�ο��𰸣�B
�������������ͼ���֪��X��Y�����ʵ������٣�Z�����ʵ������ӣ�˵��X��Y�Ƿ�Ӧ�Z���������Ӧ���е�10minʱ�����ʵ�Ũ�Ȳ��ٷ����仯��˵����Ӧ�ﵽƽ��״̬������ѡ��C����ȷ��ƽ��ʱ��Ӧ���ʲ�����0��ѡ��D����ȷ��ƽ��ʱX��Y�ֱ������1.20mol��0.40mol��0.80mol��1.00mol��0.20mol��0.80mol��Z������1.60mol�����ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪����Ӧ�Ļ�ѧ����ʽ��X + Y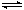 2Z��B��ȷ��A����ȷ����ѡB��
2Z��B��ȷ��A����ȷ����ѡB��
�������������е��Ѷȵ����⣬���������߿���������ǿ������������ѧ���������������ͷ�ɢ˼ά����������ʱע�����ͼ�����ʵı仯ȷ����Ӧ���������������ݱ仯��֮������Ӧ�Ļ�ѧ������֮�Ƚ��м��㡣
�����Ѷȣ�һ��
3������� ��11�֣���1��һ���¶��£��ں����ܱ�������N2O5�ɷ����� �з�Ӧ��2N2O5(g)
�з�Ӧ��2N2O5(g)  4NO2(g)��O2(g) ���SH��0
4NO2(g)��O2(g) ���SH��0
�ٷ�Ӧ�ﵽƽ�������ͨ��һ������������N2O5��ת���ʽ�?�������
����С�����䡱����
���±�Ϊ��Ӧ��T1�¶��µIJ���ʵ�����ݣ�
t/s
| 0
| 500
| 10 00 00
|
c(N2O5)/mol��L��1
| 5.00
| 3.52
| 2.48
|
��500s��N2O5�ķֽ�����Ϊ?��
����T2�¶��£���Ӧ1000sʱ���NO2��Ũ��Ϊ4.98mol/L����T2?T1����������������� �� �� =����
��2����ͼ��ʾװ�ÿ������Ʊ�N2O5����N2O5�ڵ��ص�?�� (���������������)���ɣ���缫��ӦʽΪ?��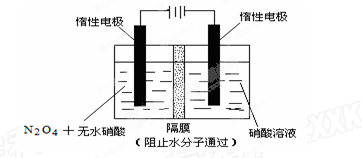
�ο��𰸣�1������? 2��? 0.00296 mol��L��1��s��1? 2��?����С�� 2��
��2������2��? N2O4��2HNO3��2e����2N2O5��2H��?3��
�����������
�����Ѷȣ�һ��
4������� ��14�֣�
(1)һ�������£������Ϊ3 L���ܱ������У�һ����̼��������Ӧ���ɼ״�(����ΪCu2O/ZnO)��CO(g)��2H2(g)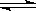 CH3OH(g)��
CH3OH(g)��
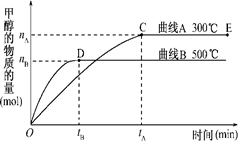
�������������ͼ��������и��⣺
�ٷ�Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ ʽK��?��
ʽK��?��
������ �¶ȣ�Kֵ??(�������С�����䡱)
�¶ȣ�Kֵ??(�������С�����䡱)
��2��һ���¶��£���3 mol A�����1 mol B����ͨ��һ�ܱ������У��������·�Ӧ��3A(g) + B(g) 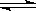 ?xC(g) ����д���пհף�����������̶�Ϊ2 L����Ӧ2 minʱ���ʣ��0.6 mol B��C��Ũ��Ϊ0.4 mol/L��
?xC(g) ����д���пհף�����������̶�Ϊ2 L����Ӧ2 minʱ���ʣ��0.6 mol B��C��Ũ��Ϊ0.4 mol/L��
��x=?
������Ӧ��4 min�ﵽƽ�⣬ƽ��ʱC��Ũ��________ 0.8 mol/L(����ڡ�������?�ڡ���С�ڡ�)��
��ƽ�������У�C���������Ϊ22%����B��ת������______________��
��3�����û�ѧ��Ӧԭ���о��������ȵ��ʼ��仯����ķ�Ӧ����Ҫ���塣
�ٺϳɰ���ӦN2 (g)+3H2(g) 2NH3(g)�����ں��¡���ѹ��������ƽ����ϵ��ͨ���������ƽ��?��
2NH3(g)�����ں��¡���ѹ��������ƽ����ϵ��ͨ���������ƽ��?�� ������������ҡ���������ʹ�ô�����������Ӧ�ġ�H________������� ����С�� ���ı䡱����
������������ҡ���������ʹ�ô�����������Ӧ�ġ�H________������� ����С�� ���ı䡱����
����������Ѱ����ʵĴ����͵缫���ϣ���N2��H2Ϊ�缫��Ӧ���HCl��NH4ClΪ�������Һ��������ȼ�յ��,�ŵ�����У���Һ��笠�����Ũ����������д���õ�ص�������Ӧʽ? ?��
?��
�ο��𰸣���14�֣�
��1����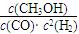 ?�ڼ�С
?�ڼ�С
��2����2(2��)��<��2�֣���36����2�֣�
��3���������ı䣨2�֣���N2+8H++6e��=2NH4+��2�֣�
�����������
�����Ѷȣ�һ��
5��ѡ���� ��֪ij�¶��£���Ӧ SO2(g)��NO2(g)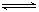 SO3(g)+NO(g)��ƽ�ⳣ��K=0.24������˵����ȷ����
SO3(g)+NO(g)��ƽ�ⳣ��K=0.24������˵����ȷ����
A�����¶��·�Ӧ2SO2(g)��2NO2(g)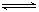 2SO3(g)+2NO(g) ��ƽ�ⳣ��Ϊ0.48
2SO3(g)+2NO(g) ��ƽ�ⳣ��Ϊ0.48
B�����÷�Ӧ��H <0���������¶Ȼ�ѧƽ�ⳣ��K��С
C���������¶ȣ��淴Ӧ���ʼ�С
D���ı�����ʹƽ�������ƶ�����ƽ��ʱn(NO2)/n(NO)һ����ԭƽ��С
�ο��𰸣�B
������������ݻ�ѧ����ʽ�ļ�������֪��ѡ��A�з�Ӧ��ƽ�ⳣ����K��0.242��ѡ��A����ȷ���������Ӧ�Ƿ��ȷ�Ӧ���������¶�ƽ�����淴Ӧ������У�ƽ�ⳣ����С��ѡ��B��ȷ�������¶ȣ����淴Ӧ���ʶ�������ģ�ѡ��C����ȷ��ѡ��D����ȷ����Ϊ����ȷ���ı�ķ�Ӧ������������ȷ�Ĵ�ѡB��
�����Ѷȣ�һ��