1、填空题 某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
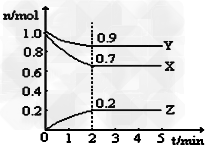
(1)该反应的化学方程式为_____________。
(2)反应开始至2min,以气体Z表示的平均反应速率为___________。
(3)2min反应达平衡,容器内混合气体的平均相对分子质量比起始时____________(填“大”,“小”或“相等”下同),混合气体密度比起始时____________。
(4)将a?mol?X与b?mol?Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n?(X)?=?n?(Y)?=?n?(Z),则原混合气体中a?:?b?=__________。
参考答案:(1)3X+Y 2Z?
2Z?
(2)0.02?mol/(L・min)或3.3×10-4?mol/(L・s)
(3)大;相等
(4)5:3
本题解析:
本题难度:一般
2、选择题 在一定温度下,向体积恒定为2L的密闭容器里充入2mol M和一定量的N,发生如下反应:M(g)+N(g) E(g);当反应进行到4min时达到平衡,测知M的浓度为0.2mol・L―1。下列说法正确的是?
E(g);当反应进行到4min时达到平衡,测知M的浓度为0.2mol・L―1。下列说法正确的是?
A.4min时,M的转化率为80%
B.4min时,用M表示这段时间内的反应速率为0.8mol・L―1・min―1
C.4min后,向容器中充入不参与反应的稀有气体,M的物质的量减小
D.2min时,M的物质的量浓度为0.6mol・L―1
参考答案:A
本题解析:平衡时M的物质的量是0.2mol/L×2L=0.4mol,所以消耗M是1.6mol,则转化率是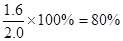 ,A正确。M的反应速率为
,A正确。M的反应速率为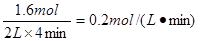 ,B不正确。体积不变,充入稀有气体,平衡不移动,所以M的物质的量不变,C不正确。反应速率在反应过程中是变化的,但不是均匀变化的,所以D不正确。答案选A。
,B不正确。体积不变,充入稀有气体,平衡不移动,所以M的物质的量不变,C不正确。反应速率在反应过程中是变化的,但不是均匀变化的,所以D不正确。答案选A。
本题难度:一般
3、选择题 在2A + B = 3C + 4D的反应中,下列表示该反应速率最大的是
[? ]
A.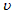 (A)=0.5 mol・L-1・min-1
(A)=0.5 mol・L-1・min-1
B.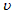 (B)=0.3 mol・L-1・min-1
(B)=0.3 mol・L-1・min-1
C.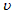 (A)=0.8 mol・L-1・min-1
(A)=0.8 mol・L-1・min-1
D.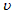 (D)=1 mol・L-1・min-1
(D)=1 mol・L-1・min-1
参考答案:C
本题解析:
本题难度:简单
4、选择题 已知可逆反应:M(g)+N(g)?P(g)+Q(g);△H>0.在某温度下,反应物的起始浓度分别为:c(M)=1mol/L,c(N)=2.4mol/L,达到平衡时N的转化率为25%.下列说法正确的是( )
A.达到平衡后,M的转化率小于25%
B.温度升高,M的体积分数增大
C.相同条件下,增大N的浓度,反应正向进行,平衡常数增大
D.相同条件下,若起始时c(M)=c(N),达到平衡后,M的转化率>25%
参考答案:M(g)+N(g)?P(g)+Q(g)
起始(mol/L):1? 2.4?0? ?0
转化(mol/L):0.6? 0.6? 0.6? ?0.6
平衡(mol/L):0.4? 1.8? ?0.6? 0.6
达到平衡后,M的转化率=0.61×100%=60%,
A.达到平衡后,M的转化率为60%,故A错误;
B.升高温度,平衡向正反应方向移动,则M的体积分数减小,故B错误;
C.相同条件下,增大N的浓度,反应正向进行,但平衡常数不变,故C错误;
D.相同条件下,若起始时c(M)=c(N),相当于在原来的基础山加入M,则达到平衡后,N的转化率>25%,M和N的转化率相等,则M的转化率>25%,故D正确.
故选D.
本题解析:
本题难度:一般
5、选择题 在一密闭容器中进行如下反应:2SO2(气)+O2(气)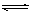 2SO3(气),已知反应过程中某一时SO2、O2、SO3,的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
2SO3(气),已知反应过程中某一时SO2、O2、SO3,的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
A.SO2为0.4mol/L、O2为0.2mol/L
B.SO3为0.4mol/L
C.SO2、S03均为0.15mol/L
D.SO2为0.25mol/L
参考答案:D
本题解析:可逆反应的特点是不可能进行到底。即反应物不可能完全转化为生成物,生成物也不可能完全转化为反应物。A若SO2为0.4mol/L则SO3为0 mol/L。错误。B SO3为0.4mol/L则SO2为0mol/L,错误。C 若SO2、S03均为0.15mol/L ,则硫原子不符合质量守恒定律,错误。D若SO2为0.25mol/L,则O2为0.125mol/L。SO3为0.15m mol/L。符合可逆反应的特点,正确。
本题难度:一般