1������� ��һ���ݻ��̶�Ϊ2L���ܱ������У�������Ӧ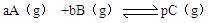 ��H=������Ӧ�����¼���±���
��H=������Ӧ�����¼���±���
ʱ��
| c��A��/mol  L-1 L-1
| c��B��/mol L-1
| c��C��/mol L-1
|
0min
| 1
| 3
| 0
|
��2m in in
| 0.8
| 2.6
| 0.4
|
��4min
| 0.4
| 1.8
| 1.2
|
��6min
| 0.4
| 1.8
| 1.2
|
��8min
| 0.1
| 2.0
| 1.8
|
��9min
| 0.05
| 1.9
| 0.3
|
?����ϸ�������ݱ������ݣ��ش��������⣺
��1��a2=?��b=?��p=?����ȡ��С��������
��2����2min����4min��A��ƽ����Ӧ����v��A��=?mol��L-1��min-1[��Դ:ѧ.��.��]
��3���ɱ������ݿ�֪��Ӧ�ڵ�4min����6minʱ����ƽ��״̬�����ڵ�2min����6min����8minʱ�ֱ�ı���ijһ��Ӧ��������ı�������ֱ�����ǣ�
�ٵ�2min ?��?
�ڵ�6min?��
�۵�8min?��
��4�����ӿ�ʼ����4min����ƽ��ʱ��Ӧ�ų�������Ϊ235��92kJ����÷�Ӧ�ġ�H=?��
2��ѡ���� T ��Cʱ����2 L�ܱ������У�X��Y��Z������������ʵ�����ʱ��仯����ͼI��ʾ������ʼʱ����һ������Y���ڲ�ͬ�¶��¸ı�X����ʱZ����������仯�����ͼII��ʾ�������н�����ȷ����
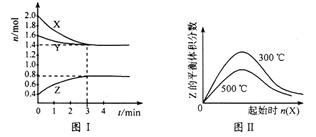
A���÷�Ӧ�Ļ�ѧ����ʽΪ�� 2X(g) + Y(g) 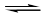 2Z(g)
2Z(g)
B����Ӧ���е�ǰ3min�ڣ���X��ʾ��ƽ����Ӧ����v(x)=0.067mol/(L��min)
C����ͼII��֪�������������䣬����X����ʱY��ת������������С
D�������������䣬���{�¶ȣ�ƽ�������ƶ�
3��ѡ���� ��Ӧ��A = 2B�У�A��B��Ũ�ȱ仯��ͼ��ʾ����2min���ڵ�ƽ����Ӧ������Ϊ�� ? ��

A��VA= 9 mol/��L��min��
B��VA= 4.5 mol/��L��min��
C��VB= 18 mol/��L��min��
D��VB= 9mol/��L��min��
4��ѡ���� ��ͼ��ʾ���淴ӦmA(g)+nB(g) pC(g)�ڲ�ͬ�¶�(T)��ѹǿ(P)�£�������C����������C%�ı仯��������й��ڸ�����Ӧ��ЧӦ������ʽ��A. B. C�Ļ�ѧ���������ж��У���ȷ����
pC(g)�ڲ�ͬ�¶�(T)��ѹǿ(P)�£�������C����������C%�ı仯��������й��ڸ�����Ӧ��ЧӦ������ʽ��A. B. C�Ļ�ѧ���������ж��У���ȷ����
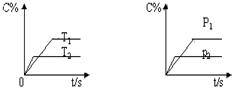
A�����ȷ�Ӧ��m+n<p? B�����ȷ�Ӧ��m+n>p
C�����ȷ�Ӧ��m+n<p? D�����ȷ�Ӧ��m+n>p
5��ѡ���� ���淴Ӧ��4A��s��+3B��g��?2C��g��+D��g�������ȷ�Ӧ����2sĩ��B��Ũ�ȼ�С0.6mol/L������˵����ȷ���ǣ�������
A����2sʱ��A��B���ʷ�Ӧ����֮��Ϊ4��3
B�������������䣬�����¶ȣ�����Ӧ���ʼ�С���淴Ӧ��������
C����2sʱ��D�����ʵ���һ������0.2mol
D�����������¶Ⱥ�������ֲ��䣬��Ӧǰ��������ѹǿ���