1������� SO2��NOx�ڻ�ѧ��ҵ������Ҫ��;��Ҳ�Ǵ�����Ⱦ����Ҫ��Դ�����������ò��أ�Ԥ�������������ǵ�ǰ��ҵ�Ϻͻ������������о�����Ҫ����֮һ��
��1���ڽӴ���������Ĺ����У�����2SO2(g)��O2(g)  2SO3(g) ��H��0��Ӧ��ij�¶��£�SO2��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ����ͼ��ʾ������ͼʾ�ش��������⣺
2SO3(g) ��H��0��Ӧ��ij�¶��£�SO2��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ����ͼ��ʾ������ͼʾ�ش��������⣺
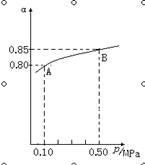
��ƽ��״̬��A��Bʱ��ƽ�ⳣ��K(A) K(B)�����������������������
�ڽ�2��0molSO2��1��0molO2����10L���ܱ������У���40s��Ӧ�ﵽƽ�⣬��ʱ��ϵ��ѹǿΪ0��10MPa����һ��ʱ����SO2��ƽ����Ӧ����Ϊ ��
�÷�Ӧ��ƽ�ⳣ��Ϊ ��
��2����CH4����ԭNOx�������������������Ⱦ�����磺CH4(g)��4NO2(g) �� 4NO(g)��CO2(g)��2H2O(g) ��H��-574kJ��mol��1
CH4(g)��4NO(g) �� 2N2(g)��CO2(g)��2H2O(g) ��H��-1160kJ��mol��1
ȡ��״����4��48LCH4��ʹ֮��ȫ��Ӧ��
������NO2��ԭ��N2������������ת�Ƶ��ӵ����ʵ���Ϊ ��
������ԭNO2��NO�Ļ����ų���������Q��ȡֵ��Χ�� ��
2��ѡ���� ��֪��Fe(s)��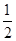 O2(g)==="FeO(s)" ��H1����272 kJ/mol
O2(g)==="FeO(s)" ��H1����272 kJ/mol
2Al(s)��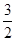 O2(g)===Al2O3(s)��H2����1 675 kJ/mol
O2(g)===Al2O3(s)��H2����1 675 kJ/mol
��2Al(s)��3FeO(s)===Al2O3(s)��3Fe(s)�Ħ�H��
A��859 kJ/mol
B����859 kJ/mol
C����1403 kJ/mol
D����2491 kJ/mol