1、选择题 常温下pH最小的是下列各项中的( )
A.pH=0的溶液
B.0.04 mol・L-1H2SO4
C.0.5 mol・L-1H Cl
D.0.05 mol・L-1CH3COOH
参考答案:A
本题解析:A项c(H+)=1 mol・L-1,B项c(H+)=0.08 mol・L-1,C项c(H+)=0.5 mol・L-1,D项c(H+)<0.05 mol・L-1,pH最小即c(H+)最大,故选A。
本题难度:一般
2、选择题 已知HF比CH3COOH易电离。关于物质的量浓度、体积都相同的NaF溶液和CH3COONa溶液,下列说法正确的是(? )
A.两溶液相比较,NaF溶液中的离子总数较多
B.在相同条件下,两溶液的pH大小为: CH3COONa< NaF
C.NaF溶液中:c(H+)+c(HF)= c(OH-)+ c(F-)
D.CH3COONa溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
参考答案:A
本题解析:A:在NaF溶液中:c(H+)+c(Na+)= c(OH-)+ c(F-)
在CH3COONa溶液中:c(H+)+c(Na+)= c(OH-)+ c(CH3COO-)
由于HF比CH3COOH易电离,则物质的量浓度、体积都相同的NaF溶液和CH3COONa溶液相比,前者的碱性弱,c(OH-)相对较小,而c(H+)相对较大,故由以上两式可知,NaF溶液中的离子总数较多,正确
B:由“越弱越水解”可知NaF溶液水解程度相对较小,pH较小,不正确
C:违反了电荷守恒,正确的为c(H+)+c(Na+)= c(OH-)+ c(F-),排除
D:由于CH3COO-部分水解,溶液呈碱性,故c(Na+)>c(CH3COO-)>c(OH-)>c(H+),排除
答案为A
本题难度:一般
3、选择题 向Cr2(SO4)3的水溶液中加入NaOH溶液,当pH =4.6时,开始出现Cr(OH)3沉淀,随着pH的升高,沉淀增多;但当pH>13时,沉淀消失,出现亮绿色的亚铬酸根离子(CrO22-)。其平衡关系如下:
Cr3++3OH- Cr(OH)3
Cr(OH)3 CrO22- + H+ + H2O
CrO22- + H+ + H2O
(紫色)?(灰绿色) (亮绿色)
向0. 05mo1・L-1 Cr2(SO4)3溶液50mL中,加入1.0mol・L-1NaOH溶液50mL,充分反应后,溶液中可观察到的现象是?(lg2=0.3)?(?)
A.溶液为紫色
B.溶液中有灰绿色沉淀
C.溶液为亮绿色
D.无法判断
参考答案:C
本题解析:Cr2(SO4)3的物质的量为0.0025mol,加入的NaOH为0.05mol,根据Cr3++3OH- Cr(OH)3可知反应后剩余的OH-为0.035mol,则c(OH-)=
Cr(OH)3可知反应后剩余的OH-为0.035mol,则c(OH-)=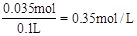 ,所以溶液的pH大于13,溶液为亮绿色。答案选C。
,所以溶液的pH大于13,溶液为亮绿色。答案选C。
点评:溶液混合时要注意混合溶液体积的变化。
本题难度:一般
4、填空题 25℃时,某酸HA:Ka=1.0×10-7,已知:溶液的酸度AG=lg[c(H+)/c(OH-)]
(1)HA的电离方程式为?。
(2)0.1 mol・L-1HA溶液中,c(H+)=?,AG=?。
(3)保持25℃,下列方法能使HA溶液的电离度、溶液pH都增大的是?(填字母)
A.加水稀释? B.加少量盐NaA固体? C.加少量NaOH固体
参考答案:(1)HA H++A-?(2)10-4mol/L? 6?(3)A C
H++A-?(2)10-4mol/L? 6?(3)A C
本题解析:
?
?试题分析:(1)由电离平衡常数可知HA为弱酸。所以HA的电离方程式为HA H++A-。(2)
H++A-。(2)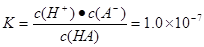 ,由于c(HA)=0. 1 mol/LHA溶液中,解得c(H+)=10-4mol/L。c(OH-)=10-10mol/L,所以AG=6.(3)保持25℃,A.加水稀释HA溶液的电离度增大,由于c(H+)减小,所以溶液pH增大。正确。B.加少量盐NaA固体,电离平衡HA
,由于c(HA)=0. 1 mol/LHA溶液中,解得c(H+)=10-4mol/L。c(OH-)=10-10mol/L,所以AG=6.(3)保持25℃,A.加水稀释HA溶液的电离度增大,由于c(H+)减小,所以溶液pH增大。正确。B.加少量盐NaA固体,电离平衡HA H++A-逆向移动,HA溶液的电离度减小,c(H+)减小,溶液pH增大。错误。C.加少量NaOH固体,电离平衡HA
H++A-逆向移动,HA溶液的电离度减小,c(H+)减小,溶液pH增大。错误。C.加少量NaOH固体,电离平衡HA H++A-正向移动,HA溶液的电离度增大,由于不断消耗H+,所以c(H+)减小,溶液pH增大。正确。考点:+)与AG的关系、外界条件对电离平衡的影响的知识。
H++A-正向移动,HA溶液的电离度增大,由于不断消耗H+,所以c(H+)减小,溶液pH增大。正确。考点:+)与AG的关系、外界条件对电离平衡的影响的知识。
本题难度:一般
5、选择题 水的电离过程为H2O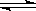 H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述不正确的是?(?)
H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述不正确的是?(?)
A.c(H+)随着温度升高而升高
B.35℃时,c(H+)>c(OH-)
C.水的电离度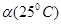 <
<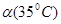
D.水的电离是吸热的
参考答案:B
本题解析:根据不同温度下水的离子积可知升高温度,平衡正向移动,所以水的电离是吸热的,c(H+)、c(OH-)随着温度升高而升高,但c(H+)=c(OH-),所以B项错误。答案选B。
点评:温度升高水的电离程度增大,但是c(H+)=c(OH-),溶液呈中性。
本题难度:一般