1、选择题 下列叙述正确的是
A.生成物总能量一定低于反应物总能量
B.放热反应速率总是大于吸热反应速率
C.形成离子键的阴、阳离子间只存在静电吸引力
D.元素周期律是元素原子核外电子排布周期性变化的结果
2、填空题 (13分)(1)“天宫一号”于2011年9月在酒泉卫星发射中心发射,标志着我国的航空航天技术迈进了一大步。火箭的第一、二级发动机中,所用的燃料为偏二甲胼和四氧化二氮,偏二甲肼可用胼来制备。
①用肼(N2H4)为燃料,四氧化二氮做氧化剂,两者反应生成氮气和气态水。
已知:N2(g)+2O2(g)=N2O4(g)?△H="10.7kJ・" mol-1[
N2H4(g)+02(g)=N2(g)+2H20(g)?△H="-543" kJ・ mol-1
写出气态肼和N2O4反应的热化学方程式为??.
②已知四氧化二氮在大气中或在较高温度下很难稳定存在,它很容易转化为二氧化氮。试推断由二氧化氮制取四氧化二氮的反应条件(或措施):?。
(2)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。如图l所示装置中,以稀土金属材料做惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y203的Zr02固体,它在高温下能传导阳极生成的02-离子(02+4e →202-)。

①c电极的名称为?,d电极上的电极反应式为?。
②如图2所示电解l00mL0.5 mol・L-1CuS04溶液,a电极上的电极反应式为?
?。若a电极产生56mL(标准状况)气体,则所得溶液的pH=?(不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入??(填序号)。
a. CuO? b. Cu(OH)2? c.CuC03? d.Cu2(OH)2C03
3、实验题 (12分)进行中和热的测定的装置如图所示。回答下列问题:
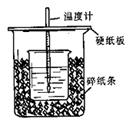
(1)从实验装置中尚缺少的一种玻璃用品是?。
(2)烧杯间填满碎纸条的作用是?。
(3)利用该装置测得的中和热数值?(填“偏大、偏小、无影响”)
(4)某研究小组将装置完善后,把V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示
(实验中始终保持V1+V2=50 mL)。回答下列问题:

①研究小组做该实验时环境温度?(填“高于”、“低于”或“等于”)22 ℃。
②由题干及图形可知,V1/V2=?:?时,酸碱恰好完全中和,此反应所用NaOH 溶液的浓度应为?mol/L。
溶液的浓度应为?mol/L。
4、选择题 下列反应中是吸热反应的是?
A.碳酸钙受热分解
B.乙醇燃烧
C.铝粉与氧化铁粉末反应
D.氧化钙溶于水
5、选择题 25℃、101kPa下,反应2N2O5(g)=4NO2(g)+O2(g)?△H=+56.7kJ/mol能自发进行的原因是)
A.是吸热反应
B.是放热反应
C.是熵减小的反应
D.熵增效应大于热效应