1、选择题 下列离子方程式中,正确的是
A.铁和氯化铁溶液的反应:Fe+Fe3+═2Fe2+
B.大理石和稀盐酸的反应:CO+2H+═CO2↑+H2O
C.碳酸氢钠溶液和氢氧化钠溶液反应:HCO+OH-═CO+H2O
D.铜和稀硝酸反应:Cu+H++NO3-=Cu2++NO↑十H2O
参考答案:C
本题解析:分析:A.电荷不守恒;
B.碳酸钙在离子反应中保留化学式;
C.反应生成碳酸钠和水;
D.电子、电荷不守恒.
解答:A.铁和氯化铁溶液的反应的离子反应为Fe+2Fe3+═3Fe2+,故A错误;
B.大理石和稀盐酸的反应的离子反应为CO32-+2H+═CO2↑+H2O+Ca2+,故B错误;
C.碳酸氢钠溶液和氢氧化钠溶液反应的离子反应为HCO3-+OH-═CO32-+H2O,故C正确;
D.铜和稀硝酸反应的离子反应为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故D错误;
故选C.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意电荷守恒、电子守恒的应用,题目难度不大.
本题难度:一般
2、选择题 Na2O2、CaC2、CaH2、Mg3N2都能与水反应,且反应中都有气体放出.下列说法正确的是
A.都是氧化还原反应
B.CaC2,Mg3N2与水反应属于复分解反应
C.Na2O2,CaH2与水反应,水作氧化剂
D.CaH2与水反应产生H2,它只是氧化产物
参考答案:B
本题解析:
本题难度:困难
3、选择题 下列叙述中正确的是( )
A.凡是强电解质在离子方程式中都要以离子的形式来表示
B.离子反应一定使溶液中所有离子的浓度都发生变化
C.复分解反应必须具备离子反应的某个条件
D.酸碱中和反应都能用离子方程式:H++OH-=H2O表示
参考答案:A、不溶性的强电解质在离子方程式的书写中要写化学式不能写离子,如碳酸钙要写化学式不能写离子,故A错误.
B、离子反应不一定使溶液中所有离子的浓度都发生变化,只有参加离子反应的离子浓度才发生变化,不参加离子反应的离子浓度不发生变化,故B错误.
C、离子反应发生的条件包含复分解反应的条件,所以复分解反应必须具备离子反应的某个条件,故C正确.
D、弱酸、弱碱的酸碱中和反应不能用离子方程式:H++OH-=H2O表示,弱酸弱碱要写化学式,故D错误.
故选C.
本题解析:
本题难度:一般
4、选择题 某溶液中,只可能含有下列离子中的几种:
现每次取100.00mL溶液进行实验:①第一份加入硝酸银溶液有沉淀产生;②第二份加入足量氯化钡溶液后得干燥沉淀6.27g,沉淀经足量盐酸洗涤,干燥后剩余2.33g。下列说法错误的是(?)
A.C( )="0.2" mol/L? B.C(K+)一定为0.6mol/L?
)="0.2" mol/L? B.C(K+)一定为0.6mol/L?
C.氯离子可能存在? D.一定有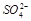 和
和
参考答案:C
本题解析:①第一份加入硝酸银溶液有沉淀产生,此沉淀不一定为氯化银,因为可能有碳酸根的存在。②第二份加入足量氯化钡溶液后得干燥沉淀6.27g,此沉淀可能是碳酸钡与硫酸钡的混合物。沉淀经足量盐酸洗涤,干燥后剩余2.33g。最后这2.33g的沉淀是硫酸钡,那么6.27-2.33=3.94g,就是碳酸钡沉淀的质量。即0.02mol,C( )="0.02mol÷0.1L=0.2" mol/L。而没有确定是否有氯离子,所以B、D选项都错,选择C。
)="0.02mol÷0.1L=0.2" mol/L。而没有确定是否有氯离子,所以B、D选项都错,选择C。
点评:本题要抓住氯离子不一定存在就可以解答,关键是熟悉离子之间的反应。属于容易题。
本题难度:一般
5、填空题 某无色溶液,其中有可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2-、S2-、CO32-、SO32- 、SO42-。现取该溶液进行有关实验,实验结果如下图所示:
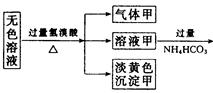
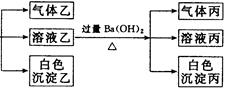
(1)沉淀甲是??,生成沉淀的离子方程式??。
(2)沉淀乙是??,由溶液甲生成沉淀乙的离子方程式??。
(3)沉淀丙是??。
(4)综合上述信息,可以肯定存在的离子有??。
参考答案:(1)S;? 2S2-+SO32-+6H+=3S↓+3H2O
(2)Al(OH)3; Al3++3HCO =Al(OH)3↓+3CO2↑
=Al(OH)3↓+3CO2↑
(3)BaCO3, 可能有BaSO4;?在沉淀丙中加入足量盐酸,若沉淀不能全部溶解,说明除BaCO3外还有BaSO4;若全部溶解,则仅有BaCO3.
(4) S2-、SO 、AlO
、AlO 、Na+
、Na+
本题解析:本题的突破口是沉淀甲、乙、丙的成分,加入过量的氢溴酸生成淡黄色沉淀甲,回顾中学化学中常见的淡黄色物质有AgBr、S、Ag3PO4等。这里应该排除排除Ag3PO4的,关键甲是AgBr还是S?若是AgBr沉淀的话,由于Ag+与题干中的4种阴离子均不能大量共存,从而否决了Ag+。可知甲是S,显然此处的S是溶液中S2-和SO32-在酸性条件下发生的归中反应生成的。由此推出原溶液中存在S2-和SO32-。由于有SO32-,所以一定不存在Ba2+、Fe3+。根据电中性原则,溶液中必须有阳离子,故一定存在Na+。气体甲可能是HBr与过量的S2-反应生成的H2S,也可能是HBr与过量的SO32-反应生成的SO2,也可能是HBr与原溶液中可能存在的CO32-反应生成的CO2。过量的NH4HCO3中和多余的H+后,又反应生成白色沉淀乙,对照题干中的离子(Ag+、Ba2+、Fe3+都不存在),推出沉淀乙只可能是Al元素引起的Al(OH)3沉淀,即HCO3-与Al3+发生双水解所造成的,而Al3+来自于AlO2-与过量的氢溴酸反应生成的,所以原溶液中一定存在AlO2-。气体乙是HCO3-与剩余的H+以及Al3+反应产生的,只能是CO2。Ba(OH)2与上步过量的NH4HCO3反应,生成白色沉淀丙,即BaCO3沉淀,另外,也可能存在BaSO4沉淀,但无法确定原溶液中是否含有CO32-和SO42-。气体丙一定是NH4+与过量的Ba(OH)2反应生成的NH3。
综上所述,肯定存在的离子有:Na+、AlO2-、S2-、SO32-;一定不存在的离子有:Ag+、Ba2+、Fe3+;可能存在的离子有:CO32-、SO42-。
本题难度:一般