1、选择题 工业合成氨中,N2(g)+3H2(g)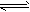 2NH3(g),其△H<0,常采用700k左右的温度条件,其原因是
2NH3(g),其△H<0,常采用700k左右的温度条件,其原因是
[? ]
A.加快反应速率
B.提高原料的转化率
C.使平衡向合成氨的方向移动
D.使催化剂的活性达到最佳状态
参考答案:AD
本题解析:
本题难度:一般
2、填空题 (1)已知16g固体单质S完全燃烧生成SO2气体时,放出148.4kJ的热量,则该反应的热化学方程式为
_______________________。
(2)NH3水溶液呈弱碱性,并可用作农业化肥,现进行下列研究:现将一定量的H2和N2充入10L的密闭容器中,在一定条件下使其发生反应,有关H2、N2、NH3三者的物质的量的变化与时间的关系如图所示
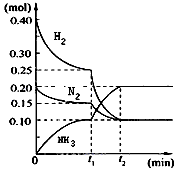
若t1=10min,则0至t1时间内H2物质的反应速率为_____________;该反应在t2时达到平衡,其化学反应方程式为___________,此温度下该反应的平衡常数为_____________。试判断t1时反应是否处于平衡状态____________(是或否)原因是_________________。
根据图中曲线变化情况判断,t1时刻改变的反应条件可能是______________(填下列各项序号)
a.加入了催化剂 b.降低了反应的温度 c.向容器中又充入了气体N2
参考答案:(1)S(s)+O2(g)=SO2(g) △H =-296.8kJ・mol-1
(2)0.0015mol・L-1・min-1; N2+3H2 2NH3;4×102(mol・L-1)-2;否;浓度商不等于4×102;a
2NH3;4×102(mol・L-1)-2;否;浓度商不等于4×102;a
本题解析:
本题难度:一般
3、简答题 向一个容积为5L的密闭容器中充入NH3和O2,它们的物质的量之比为1:2,发生如下反应:
4NH3(g)+5O2(g)?4NO(g)+6H2O(g)
(1)上述反应平衡常数的表达式为______;
(2)上述反应在一定条件下2min后达到平衡,NH3为2mol,NH3的转化率为20%.用NO的浓度变化表示该反应的平均反应速率为______,O2的平衡浓度为______;
(3)在达到平衡后,加入相当于原组成气体1倍的惰性气体.如果容器的体积不变,平衡______移动(填“正向”、“逆向”或“不”,下同),如果总压强保持不变,平衡______移动.
参考答案:(1)平衡常数表达式为生成物浓度的幂之积与反应物浓度幂之积的比值,K=c4(NO)c6(H2O)c4(NH3)c5(O2),
故答案为:c4(NO)×c6(H2O)c4(NH3)×c5(O2)
(2)设充入NH3为xmol,
4NH3(g)+5O2(g)?4NO(g)+6H2O(g)
加入量 x 2x 0 0
反应量0.2x0.25x 0.2x 0.3x
平衡量22x-0.25x0.2x 0.3x
2min后达到平衡,NH3为2mol,NH3的转化率为20%,
x-0.2x=2,
解得x=2.5
用NO的浓度变化表示该反应的平均反应速率为0.2×2.5mol5L2min=0.25mol?L-1?min-1,
O2的平衡浓度为2×2.5mol-0.25×2.5mol5L=0.875mol?L-1,
故答案为:0.25mol?L-1?min-1;0.875mol?L-1 ;
(3)容积不变通入惰性气体,因为浓度不变,平衡不移动;当压强不变通入惰性气体时体积会增大,各气体的分压会变小,相当于压强减小,平衡将向气体系数之和大的一方移动,即向正向移动,
故答案为:不;正向.
本题解析:
本题难度:一般
4、选择题 下列图象能正确地表达可逆反应3A(g)+B(g)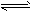 2C(g)(ΔH<0)的是
2C(g)(ΔH<0)的是
[? ]
A.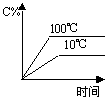
B.
C.
D.
参考答案:D
本题解析:
本题难度:一般
5、选择题 在恒温条件下,将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,测得各物质的浓度随时间变化关系如下图所示 下列说法正确的是

[? ]
A.图中的两条曲线中,Y是表示NO2浓度随时间的变化曲线
B.前10 min内,用v(NO2)表示的化学反应速率为0. 06 mol/(L・min)
C.在25 min时,反应改变的条件是增大了NO2的浓度
D.a、b、c、d四个点中,有a、b、d点的化学反应处于平衡状态
参考答案:C
本题解析:
本题难度:一般