1、填空题 (1)氮的氢化物肼(N2H4)是航天火箭发射常用的燃料 ?
①发射火箭时肼(N2H4)为燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知4gN2H4(g)在上述反应中放出71kJ的热量,写出该反应的热化学方程式_________。 ?
?②工业上可采用电化学的方法获得N2H2,装置如图,则通入氨气一极的电极反应式为_______________。?
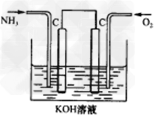
③将标准状况下112?mL?CO2通入100?mL?0.1?mol/L的氨水中,所得溶液pH=10,则溶液中离子浓度以大到小的顺序___________。该溶液中:c(HCO3-)+c(CO32- )+c(H2CO3)=___________(忽略溶液体积的变化)。 ?
(2)T℃下,某2L容器内A、M、N三种物质参与的某一化学反应:
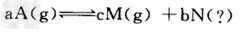 ?
?
①其物质的量随反应时间的变化的曲线如图,此反应0~5min反应物A的反应速率为__________;若达到平衡后移走1mol?A,再次达平衡后M小于0.75?mol,则该反应在T℃的化学平衡常数为___________。?
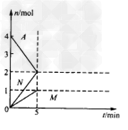
②若为了寻找该反应的最佳条件,在反应过程中持续不断地升高温度,所得的M的体积分数如下图,则温度T1和T2下化学平衡常数 K1___________K2(填“>”、“<”“=”)
2、填空题 将两支惰性电极插入500mLAgNO3溶液中,通电电解,当电解液的pH由6.0变为3.0时(设电解时阴极没有氢析出,且电解液在电解前后体积变化可以忽略)。
(1)写出电极反应式阳极:______________, 阴极:______________。
(2)电极上应析出银的质量是_______________。
(3)欲使该溶液复原应加入_______________________。
3、填空题 目前高铁酸钠(Na2FeO4)被广泛应用于水处理,具有高效、无毒的优点。
(1)?将Fe(OH)3与NaClO溶液混合,可制得Na2FeO4,完成并配平下列离子方程式

(2)?用Fe做阳极,Cu做阴极,NaOH溶液做电解液,用电解的方法也可制得Na2FeO4,则电解过程中阳极的反应式为______________________
(3)?某地海水样品经Na2FeO4处理后,所含离子及其浓度如下表所示(H+和OH-未列出):
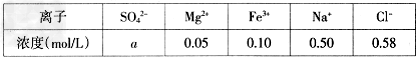
常温下,取一定量经Na2FeO4处理过的海水为原料制备精制食盐水和MgCl2・7H2O,过程如下

注:离子的浓度小于?,可认为该离子不存在;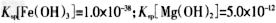 ;操作过程中溶液体积的变化忽略不计。
;操作过程中溶液体积的变化忽略不计。
①表格中的a_______0.16?(填“”或“=”)。
②沉淀A的组成为_______?(填化学式);在调节溶液PH时,理论上应调节的pH的范围是_____________________
③加入的过量试剂X为_______?(填化学式)。
④加入过量HCl的作用为______________
4、填空题 在25℃时,用石墨电极电解1.0L 2.5mol/LCuSO4溶液。5min后,在一个石墨电极上有3.2gCu生成。
试回答下列问题:
(1)________极发生氧化反应,电极反应式为___________________
(2)有________mol电子发生转移,得到O2的体积(标准状况)是________mL,溶液的pH是________
(3)如用等质量的两块铜片代替石墨作电极,电解相同时间后两铜片的质量相差________g,电解液的
pH________(填“变小”.“变大”或“不变”)
5、填空题 钛是一种重要的金属,工业上用钛铁矿(FeTiO3,含FeO、Al2O3、SiO2等杂质)为原料制钛白粉(
TiO2),TiO2常通过两种方法还原制得Ti。

已知:2H2SO4+FeTiO3==TiOSO4+FeSO4 +2H2O. 回答下列问题:
(1)净化钛矿石时,需用浓氢氧化钠溶液来处理,该过程中发生反应的化学方程式有:
SiO2+2NaOH=Na2SiO3+ H2O和___。
(2)滤液①中的溶质主要是FeSO4,检验其中Fe2+的方法是___。
(3) TiOSO4是一种强酸弱碱盐。从TiOSO4→H2TiO3需要加热,则加热的目的是____。
(4)电解TiO2来获得Ti是以TiO2作阴极,石墨作阳极,熔融CaO为电解液,用碳块作电解槽。其阴极反应的电极反应式为___。
(5)因为反应TiO2(s)+2Cl2(g)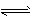 TiCl4(l)+O2(g) △H=+151 kJ.mol-1难于发生,所以工业上不能直接由TiO2和
TiCl4(l)+O2(g) △H=+151 kJ.mol-1难于发生,所以工业上不能直接由TiO2和
Cl2反应来制取TiCl4。当反应体系中加入炭粉后,反应分如下两步进行:
2C(s) +O2 ( g)=2CO( g) △H1= -221 kJ . mol-1
TiO2(s) +2C(s) +2Cl2(g)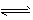 TiCl4 (l) +2CO( g) △H2 则△H2=____。
TiCl4 (l) +2CO( g) △H2 则△H2=____。