1、选择题 下图中正确的是? ( )。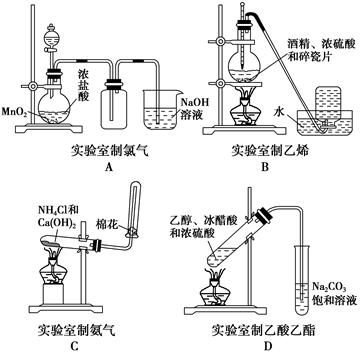
参考答案:C
本题解析:实验室常用MnO2与浓盐酸加热制备Cl2,故A错误;乙醇和浓硫酸脱水制备乙烯,需要控制反应温度为170 ℃,温度计水银球应没于液面下,故B错误;实验室制备乙酸乙酯时,导气管不能伸入Na2CO3饱和溶液液面下,故D错误。
本题难度:一般
2、选择题 下列离子中,可以用焰色反应来鉴别的是
A.Na+
B.NH4+
C.CO32―
D.Cl―
参考答案:A
本题解析:焰色反应是化学上用来测试某些金属元素是否存在的方法,所以A正确。
点评:熟记焰色反应定义及常见金属的焰色反应现象,此题属于简单题型
本题难度:简单
3、选择题 设NA为阿伏加德罗常数的值,下列有关说法不正确的是
A.标准状况下,48gO3含有的氧原子数是3NA
B.含107gFe(OH)3的胶体中胶粒总数是NA
C.0.5L0.2mol?L-1的NaCl溶液中含有的Na+是0.1NA
D.标准状况下,33.6LCO中含有的原子数是3NA
参考答案:B
本题解析:分析:A、根据n= 计算氧原子物质的量,再根据N=nNA计算氧原子数目.
计算氧原子物质的量,再根据N=nNA计算氧原子数目.
B、Fe(OH)3的胶体中胶粒是Fe(OH)3集合体.
C、根据n=cV计算钠离子的物质的量,再根据N=nNA计算钠离子数目.
D、根据n= 计算一氧化碳的物质的量,再根据N=nNA计算原子数目.
计算一氧化碳的物质的量,再根据N=nNA计算原子数目.
解答:A、标准状况下,48gO3含有的氧原子数为 ×3×NAmol-1=3NA,故A正确;
×3×NAmol-1=3NA,故A正确;
B、Fe(OH)3的胶体中胶粒是Fe(OH)3集合体,故B错误;
C、0.5L0.2mol?L-1的NaCl溶液中含有的Na+是0.5L×0.2mol?L-1×NAmol-1=0.1NA,故C正确;
D、标准状况下,33.6LCO中含有的原子数是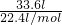 ×2×NAmol-1=3NA,故D正确.
×2×NAmol-1=3NA,故D正确.
故选:B.
点评:考查常用化学计量数的有关计算,难度较小,注意胶体中胶粒是许多粒子集合体.
本题难度:简单
4、选择题 铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混和、压制,就可以制成铅笔芯。如果铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1mg。那么一个铅笔字含有的碳原子数约为?
A.2.5×1019个
B.2.5×1022个
C.5×1019个
D.5×1022个
参考答案:A
本题解析:试题分析:首先计算写一个字所含石墨的质量为0.5mg,则含C原子的物质的量为0.5×10-3/12,则碳原子的个数=5×10-4/12×6.02×1023=2.5×1019个。
考点:物质分子中的原子个数计算;阿伏加德罗常数
点评:考查物质中原子数目及常用化学计量计算,比较基础,注意公式的灵活运用。
本题难度:困难
5、实验题 碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的、以化合态形式存在的碘元素。在实验室中,从海藻里提取碘的流程和实验装置如下:
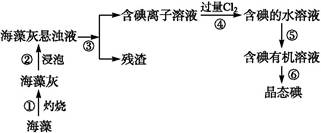
(1)指出上述提取碘的过程中有关实验操作的名称:步骤③ ,步骤⑤ 。?
(2)写出步骤④对应反应的离子方程式: 。?
(3)提取碘的过程中,可供选择的有机试剂是 。(填编号)?
A.酒精? B.醋酸? C.四氯化碳? D.苯
(4)步骤④除了加入过量Cl2,下列氧化剂最好选用 (填代号)。?
A.浓硫酸? B.H2O2溶液? C.KMnO4溶液
理由是____________________________。?
(5)为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至⑤,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器和物品,尚缺少的玻璃仪器是 。?
(6)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出下图实验装置中存在的错误之处: 。?
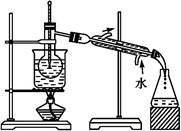
参考答案:(1)过滤 萃取、分液(每空1分)
(2)Cl2+2I- I2+2Cl-(2分)
I2+2Cl-(2分)
(3)CD(1分)
(4)B(1分)
过氧化氢是绿色氧化剂,在氧化过程中不会引进杂质,也不产生污染(2分)
(5)分液漏斗、普通漏斗(2分)
(6)温度计水银球的位置不对(2分)
本题解析:(1)从流程图中可知操作③是过滤,操作⑤是萃取、分液。(2)Cl2的氧化性大于I2,可发生反应Cl2+2I- I2+2Cl-。(3)根据萃取原理,要从含碘的水溶液中萃取碘,所选萃取剂一定要和水互不相溶或很难相溶,且溶质在萃取剂中溶解度要比在水中大得多。在选项中酒精、醋酸皆与水互溶。因此C、D正确。(4)氧化剂选过氧化氢,因为它是绿色氧化剂,反应过程中无污染物产生。(5)按照流程图考虑每一步需要的仪器还缺少普通漏斗和分液漏斗。(6)检查实验装置的错误,要按实验进程逐一检查。由图示装置可看出温度计水银球的位置不对。
I2+2Cl-。(3)根据萃取原理,要从含碘的水溶液中萃取碘,所选萃取剂一定要和水互不相溶或很难相溶,且溶质在萃取剂中溶解度要比在水中大得多。在选项中酒精、醋酸皆与水互溶。因此C、D正确。(4)氧化剂选过氧化氢,因为它是绿色氧化剂,反应过程中无污染物产生。(5)按照流程图考虑每一步需要的仪器还缺少普通漏斗和分液漏斗。(6)检查实验装置的错误,要按实验进程逐一检查。由图示装置可看出温度计水银球的位置不对。
本题难度:一般