1、选择题 25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH 的关系如右图所示。下列有关溶液中离子浓度关系叙述正确的是(?)

A.W点所示的溶液中:c(Na+)+ c(H+)=2c(CO32-)+ c(OH-)+ c(Cl-)
B.pH=4的溶液中:c(H2CO3)+ c(HCO3-)+ c(CO32?-)<0.1 mol・L-1
C.pH=8的溶液中:c(H+)+ c(H2CO3)+ c(HCO3-)=c(OH-)+c(Cl-)
D.pH=11的溶液中:c(Na+)>c(Cl-)>c(CO32?-)>c(HCO3-)>c(H2CO3)
2、选择题 下列说法不正确的是
[? ]
A.下列事实不能用勒夏特列原理解释:
①铁在潮湿的空气中生锈
②2HI(g)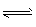 I2(g)+H2(g)达平衡,将体积缩小为原来的1/2,气体颜色加深
I2(g)+H2(g)达平衡,将体积缩小为原来的1/2,气体颜色加深
B.加入浓的NH4Cl溶液,会使Mg(OH)2的溶解沉淀平衡向溶解的方向移动
C.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小
D.用氢氧化钠溶液滴定未知浓度的盐酸,碱式滴定管滴定前读数时仰视,结束时读数平视,导致滴定结果偏小
3、选择题 0.1 mol/L NaOH和0.1 mol/L NH4Cl溶液等体积混和后,离子浓度大小顺序正确的是
A.c(Na+)>c(Cl-)>c(OH-)>c(H+)
B.c(Na+)=c(Cl-)>c(OH-)>c(H+)
C.c(Na+)=c(Cl-)>c(H+)>c(OH-)
D.c(Cl-)>c(Na+)>c(OH-)>c(H+)